Хирургическая техника робот-ассистированной сакрокольпопексии
Введение
Нет сомнения в том, что за последние десятилетия самой масштабной технологической разработкой стал хирургический робот Da Vinci, который расширяет как географическую, так и хирургическую области применения [1]. Число робот-ассистированных (РА) вмешательств за 2018 г. превысило 1 млн и неуклонно растет.
Использование робота в хирургической практике имеет ряд преимуществ по сравнению с открытым доступом, включая следующие:
- 3D-изображение высокой четкости (HD) с интегрированным освещением, системой управления фокусом и автоматическим определением оперативного поля, обеспечивающее лучшую визуализацию анатомических структур в ходе операции.
- Роботические руки, масштабируя и преобразуя движения кистей оперирующего хирурга, позволяют производить прецизионные и маневренные действия, что дает возможность оперировать в трудоемких пространствах, доступных зачастую лишь при открытой хирургии [2].
- Минимизация прямого контакта с пациентом позволяет снизить риск передачи гематогенных инфекций.
- Использование робота упрощает оперативные вмешательства у пациенток с ожирением [3—5].
- Эргономика роботической установки позволяет снизить нагрузку на скелетно-мышечную систему хирурга, особенно при продолжительных операциях [6, 7].
Апикальная поддержка является ключевой в хирургической коррекции пролапса тазовых органов [8]. Сакрокольпопексия (SCP) сохраняет статус «золотого стандарта» при лечении пациенток с апикальным пролапсом гениталий [9]. Данная операция анатомически и патогенетически обоснованна за счет обеспечения I и II уровней поддержки тазового дна по классификации DeLancey [10]).
SCP была впервые представлена в Париже абдоминальным доступом в 1957 г. С 90-х годов XX века данная операция адаптирована под мини-инвазивный доступ A. Wattiez [11] — она объединила высокую эффективность промонтофиксации с преимуществами лапароскопии. Однако данный доступ при выполнении SCP имеет ряд таких недостатков, как длительная «кривая обучения» [12], лимитированный объем движений рук хирурга и тактильного восприятия. Все это может приводить к увеличению продолжительности операции, что негативно влияет на ее широкое внедрение. Роботохирургия наиболее приемлема для проведения SCP ввиду необходимости работы в труднодоступных пространствах малого таза, наложения большого количества швов и продолжительности операции.
Показания к SCP: изолированный апикальный пролапс тазовых органов II—IV стадии по классификации Pelvic Organ Prolapse Quantification (POP-Q) или таковой в сочетании с ректоцеле. Данная операция наиболее предпочтительная у молодых и активных в половом поведении женщин, поскольку использование вагинальных синтетических протезов в подобной ситуации сопряжено с высоким риском формирования mesh-ассоциированных осложнений [13].
Хирургическая техника роботической сакрокольпопексии. Литотомическое положение пациентки на операционном столе. Катетеризация мочевого пузыря катетером Фолея. Правосторонний боковой «докинг» при данной операции предпочтителен, так как обеспечивает доступ ассистенту для выполнения манипуляций вагинальным доступом, а также со стороны дополнительного ассистентского порта в левой подвздошной области.
Размещение троакаров на расстоянии 8 см друг от друга направлено на достижение максимальной амплитуды движений роботических «рук» и предотвращение их интраоперационного «конфликта». Используются оптический троакар (12 мм) и 4 дополнительных троакара (3 из них диаметром 8 мм и один ассистентский троакар диаметром 11 мм). Оптический троакар устанавливается в точке на 2 см выше пупочного кольца. Первые два роботических троакара располагаются латеральнее оптического на расстоянии как минимум 8 см друг от друга во избежание последующей коллизии механизмов. Третий роботический, а также лапароскопический ассистентский порты устанавливаются согласно предыдущему правилу, формируя латинскую букву W (рис. 1).
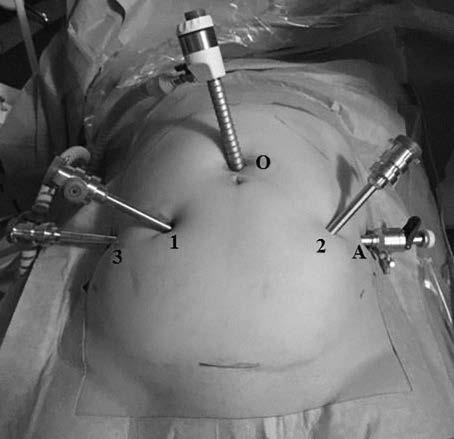
Рис. 1. Расположение портов при робот-ассистированной сакрокольпопексии.
О — оптический троакар; 1, 2, 3 — дополнительные роботические троакары; А — ассистентский троакар.
Для операции используются следующие инструменты: биполярный зажим, ножницы с возможностью применения монополярного разрезания и коагуляции, атравматичный окончатый зажим, два иглодержателя, один из которых имеет лезвия в о сновании бранш (рис. 2). Для ассистенции вагинальным доступом применяются вагинальный зонд или маточный манипулятор (рис. 3).
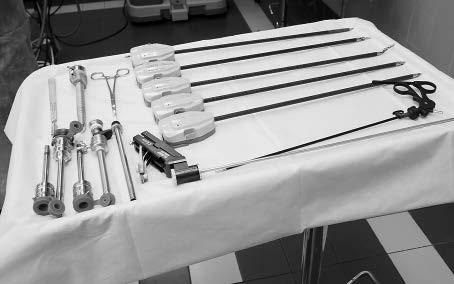
Рис. 2. Набор инструментов для проведения робот-ассистированной сакрокольпопексии.
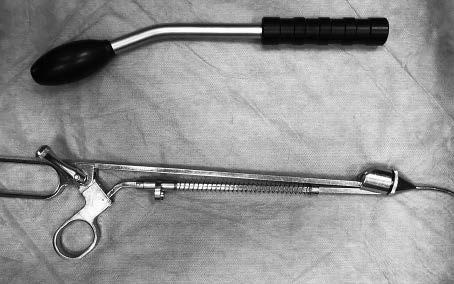
Рис. 3. Спектр манипуляторов для вагинальной ассистенции при робот-ассистированной сакрокольпопексии.
Выделяют следующие хирургические этапы робот-ассистированной сакрокольпопексии (RA SCP) (рис. 4 на цв. вклейке).
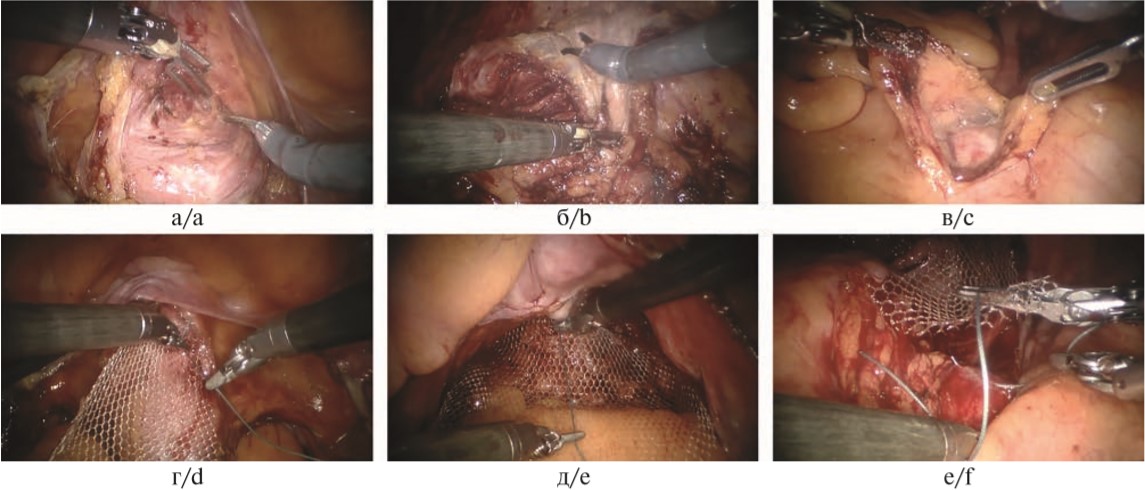
Рис. 4. Этапы выполнения робот-ассистированной сакрокольпопексии.
а — вскрытие париетальной брюшины с мобилизацией передней стенки влагалища и мочевого пузыря; б — вскрытие париетальной брюшины дугласова пространства с мобилизацией промежностного тела и мышц, поднимающих задний проход; в — вскрытие париетальной брюшины в проекции продольной пресакральной связки; г — фиксация передней части сетчатого протеза к передней стенке влагалища; д — фиксация задней части сетчатого протеза к промежностному телу; е — фиксация протеза к продольной пресакральной связке в области крестцового мыса.
I этап. Широко вскрывают париетальную брюшину дугласова пространства, разрез продлевают справа, медиальнее брыжейки сигмовидной кишки до проекции продольной пресакральной связки на уровне крестцового мыса (см. рис. 4в на цв. вклейке). Предварительная идентификация анатомических ориентиров позволяет обезопасить ход операции (правый мочеточник, правые общая и внутренняя подвздошные артерии, срединная сакральная артерия и вена). Затем тупым путем производят диссекцию ректовагинального клетчаточного пространства с целью выделения средних порций лобково-прямокишечных мышц и ректовагинальной перегородки до уровня промежностного тела (см. рис. 4б на цв. вклейке). После вскрытия пузырно-маточной складки переднюю стенку влагалища отделяют от задней стенки мочевого пузыря до уровня его шейки с обязательным сохранением целостности лобково-шеечных связок (см. рис. 4а на цв. вклейке). При наличии тела матки после данного этапа предпочтительно выполнение супрацервикальной гистерэктомии с формированием культи шейки матки монофиламентными узловыми швами.
II этап. Из полипропиленового материала с индексом soft выкраивают 2 лоскута особой формы: задний размерами 15×8 см, передний — 5×3 см (рис. 5). Нерассасывающимся плетеным шовным материалом (Ethibond) края первого лоскута фиксируют к средней порции лобково-прямокишечных мышц (пучок мышц, поднимающих задний проход) с обеих сторон, а также к промежностному телу (см. рис. 4д на цв. вклейке). При этом фиксацию выполняют на глубину до 5 мм в связи с риском травматизации полового нерва, который располагается в области проекции наружной стенки седалищно-прямокишечной ямки в расщеплении фасции внутренней запирательной мышцы (канал Алькока). Край первого лоскута после предварительной идентификации мочеточников также фиксируют к крестцово-маточным связкам и задней поверхности шейки матки или куполу влагалища. Фиксацию края второго лоскута выполняют к передней стенке влагалища (см. рис. 4г на цв. в клейке), передней поверхности культи шейки матки или куполу влагалища, а также к первому лоскуту отдельными нерассасывающимися лигатурами. Расстояние между швами на передней и задней стенках влагалища должно составлять 2,5 см и 3,5 см соответственно.
III этап. Свободный конец заднего лоскута в состоянии умеренного натяжения фиксируют нерассасывающимся шовным материалом к продольной пресакральной связке (см. рис. 4е на цв. вклейке), в результате чего протез приобретает Y-образную форму (рис. 6).
Рис. 5. Задний и передний лоскуты протеза, используемые при сакрокольпопексии.
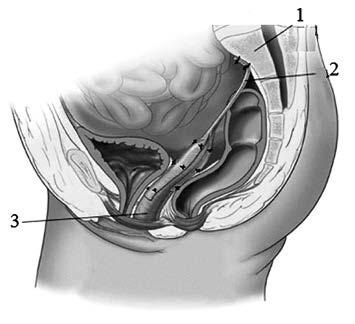
Рис. 6. Конечный вид протеза при сакрокольпопексии.
1 — крестец, 2 — сетчатый протез, 3 — влагалище.
IV этап. Производят перитонизацию сетчатого протеза непрерывным рассасывающимся швом, обеспечивая его ретроперитонеальное расположение. По окончании операции обязательно проведение тампонады влагалища марлей, смоченной антисептическим раствором.
Обсуждение
С января 2013 г. по декабрь 2019 г. в Московском областном НИИ акушерства и гинекологии роботассистированная сакрокольпопексия произведена у 181 пациентки. Средняя продолжительность операции составила 158±37,27 мин (p<0,05). Все пациентки наблюдались в поликлиническом отделении в течение 1 года после операции. Отдаленные результаты (более 1 года после вмешательства) оценены у 74 пациенток. Ни у одной их них не обнаружено mesh-ассоциированных осложнений, требующих хирургической коррекции.
Субъективное улучшение оценено при помощи специальных анкет: PFDI-20 (Pelvic Floor Distress Inventory), PFIQ-7 (Pelvic Floor Impact Questionnaire) и PISQ-12 (Pelvic Organ Prolapse/Urinary Incontinence Sexual Questionnaire). Отличный и хороший субъективный результат, отраженный улучшением результатов прохождения опросников, отметили 70 (94,6%) пациенток.
Оценка анатомических результатов проводилась путем вагинального осмотра с применением системы POP-Q. У 61 (82,4%) пациентки отмечен хороший и отличный результат операции, заключающийся в отсутствии рецидива пролапса или наличии такового I стадии. Однако у 13 (17,6%) женщин выявлен рецидив опущения половых органов II—III стадии, проявившийся исключительно в форме цистоцеле. Только 2 (2,7%) больных была произведена хирургическая коррекция пролапса повторно (SCP и вагинальная кольпопексия системой OPUR).
Заключение
Робот-ассистированная сакрокольпопексия — это операция выбора у живущих половой жизнью женщин с апикальным пролапсом гениталий. Использование робота в хирургической практ ике приоритетно у пациенток с ожирением, выраженным спаечным процессом, а также с рецидивными формами пролапса гениталий после коррекции опущения тазовых органов сетчатыми протезами как вагинальным, так и лапароскопическим доступами.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.







