Роботическая «рукавная гастрэктомия»: опыт клиники
Введение
Трудности, с которыми сталкиваются хирурги, оперирующие пациентов с ожирением, включают в себя работу с выраженной подкожно-жировой клетчаткой передней брюшной стенки и ограниченное пространство для маневрирования инструментами из-за увеличенной левой доли печени и с большим количеством внутрибрюшной жировой ткани. Робот Da V inci («I ntuitive Surgical», США), являясь дополнением к арсеналу минимально инвазивных хирургов, по-видимому, идеально подходит для работы с такими пациентами [1]. Сложные длительные операции с формированием анастомозов, такие как желудочное шунтирование Roux-en-Y, вероятно, будут более очевидным преимуществом робота перед стандартной лапароскопией [2]. Роботизированная хирургия отличается от лапароскопической тем, что хирург имеет возможность управлять камерой и инструментами дистанционно. Эргономика роботизированной платформы приводит к меньшей утомляемости хирурга по сравнению с лапароскопической техникой [3]. Хирург получает 3D-изображение, а инструменты находятся под запястьем, что обеспечивает большую свободу движений и ловкость рук для выполнения хирургических задач, таких как формирование интракорпоральных швов [4, 5]. Однако при этом теряется тактильная обратная связь, которая частично компенсируется визуальной картиной [6]. Еще одним недостатком роботизированной операции считается увеличение продолжительности вмешательства из-за времени, затрачиваемого на настройку роботической системы. Роботизированные хирургические системы Da Vinci требуют бол́ьших затрат, связанных с обслуживанием комплекса и использованием расходных материалов. Экономическая эффективность роботической системы при бариатрических вмешательствах до конца не изучена [7].
«Рукавная гастрэктомия» может считаться идеальной обучающей операцией для введения робота в бариатрическую хирургическую практику, так как представляет собой стандартизированное вмешательство [8, 9] и признается экспертами в качестве обучающей операции для роботизированной хирургии [10]. «Рукавная гастрэктомия» как операция, выполняемая в одном квадранте, позволяет хирургу привыкнуть к роботизированной платформе и свойствам обработки тканей различными роботическими инструментами, не имеющими тактильной обратной связи. Операционная и расположение пациента для роботической «рукавной гастрэктомии» также могут быть применимы для других хирургических операций на верхних отделах желудочно-кишечного тракта, таких как желудочное шунтирование, операции при грыже пищеводного отверстия диафрагмы (фундопликация) и операции при ахалазии кардии. Дополнительные операции, такие как адгезиолизис и холецистэктомия, могут еще больше расширить оперативный опыт хирурга при проведении «рукавной гастрэктомии» с использованием роботической платформы.
Если обратиться к литературе, то в российской хирургической практике можно найти достаточное количество работ, посвященных применению роботических технологий в абдоминальной хирургии, в частности в хирургии поджелудочной железы [11, 12], хирургии прямой кишки [13], хирургической онкогинекологии [14] и т.д., чего нельзя сказать о работах по бариатрической роботической хирургии. Цель данного исследования — продемонстрировать безопасный способ внедрения новой технологии, робота Da Vinci, в устоявшуюся хирургическую практику и в бариатрической хирургии тоже.
Материал и методы
Данное исследование было проведено как ретроспективный обзор проспективно поддерживаемой базы данных. В период с марта 2020 г. по февраль 2023 г. первые 15 случаев роботической «рукавной гастрэктомии» были выполнены постоянной командой хирургов (оператор консоли и хирург-ассистент) и внесены в проспективную базу данных. Все пациенты на дооперационном этапе были рассмотрены мультидисциплинарной командой (хирург, гастроэнтеролог-диетолог, эндокринолог, сомнолог и психолог) до операции и имели индекс массы тела (ИМТ) >40 кг/м2 или ИМТ >35 кг/м2 с сопутствующими ожирению заболеваниями. Эти случаи составляют основу настоящего анализа.
Подготовка к операции
Расположение в операционной показано на рис. 1. Пациента уложили в обратное положение Тренделенбурга (положение «пляжного кресла»), при этом левая рука вытянута вбок, а правая — лежит на подлокотнике.
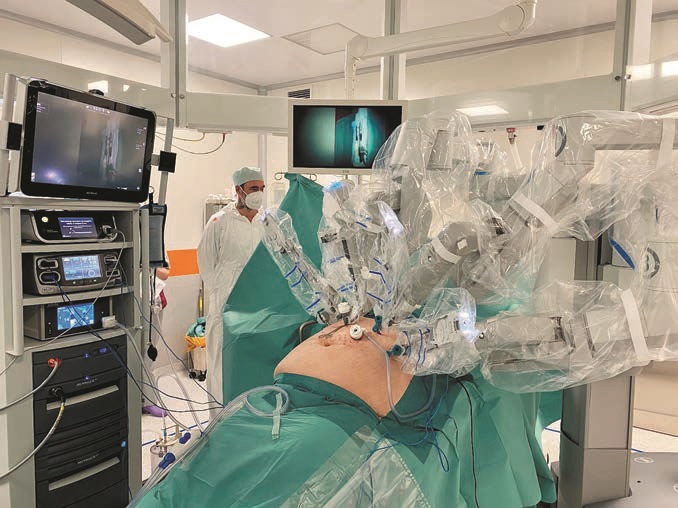 Рис. 1. Фотография положения на операционном столе относительно роботической консоли-пациента.
Рис. 1. Фотография положения на операционном столе относительно роботической консоли-пациента.
Докинг (установка консоли пациента)
Первоначальный доступ в брюшную полость осуществляли на 16 см ниже мечевидного отростка по средней линии с помощью удлиненной иглы Вереша. Устанавливали первый троакар 12 мм с 30-градусной камерой Da Vinci. Инсуффляцию CO2 проводили до 12—14 мм рт.ст. Порты и печеночный ретрактор StrongArm Nathanson Hook («Mediflex Surgical Products», США) были установлены как показано на рис. 2. Затем консоль пациента подвозилась к его левому плечу (см. рис. 1), и производился докинг.
Операция начиналась с деваскуляризации/мобилизации большей кривизны желудка с помощью ультразвукового роботического скальпеля Harmonic, при этом рассечение начинали на 2—3 см проксимальнее привратника (рис. 3) до левой ножки диафрагмы (рис. 4). При наличии грыжи пищеводного отверстия диафрагмы производили крурорафию.
Затем анестезиолог проводил желудочный зонд диаметром 36 Fr до привратника под визуальным и инструментальным контролем. Прошивание и пересечение желудка выполняли через порт ассистента с помощью электрического ретикулярного линейного степлера Echelon Flex длиной 60 мм с высотой открытой скобы 4,1 мм (зеленая кассета) для всех прошиваний (рис. 5). Каждый раз перед прошиванием степлером достигали 60-секундное время сжатия. Положение сшивающего аппарата было «свободным» на зонде, а последнее прошивание направлено на левую ножку диафрагмы, обеспечивая захват всего дна желудка с отступом около 1 см от области пищеводно-желудочного перехода.
Линия степлерного шва была ушита во всех случаях рассасывающимся шовным материалом (V-lock 180 размером 3,0, длиной 30 см) (рис. 6).
Хирург у операционного стола через порт ассистента производил извлечение резецированного желудка, к зоне операции устанавливали страховочный дренаж, затем апоневроз в области ассистентского и оптического троакарных доступов ушивали с помощью иглы Берси.
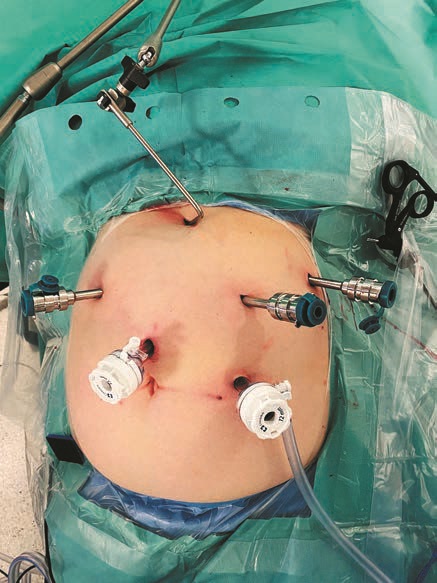 Рис. 2. Фотография расположения троакаров в передней брюшной стенке.
Рис. 2. Фотография расположения троакаров в передней брюшной стенке.
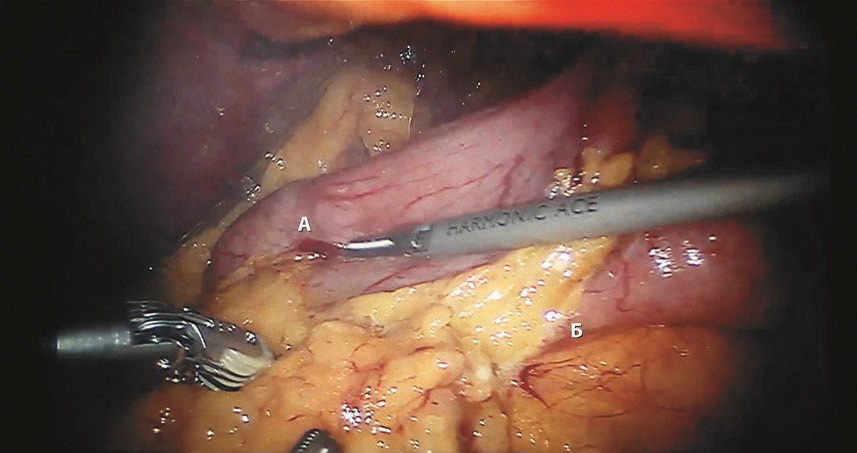 Рис. 3. Мобилизация желудка в области привратника.
Рис. 3. Мобилизация желудка в области привратника.
А — привратник; Б — область мобилизации (3 см от привратника). Интраоперационная фотография.
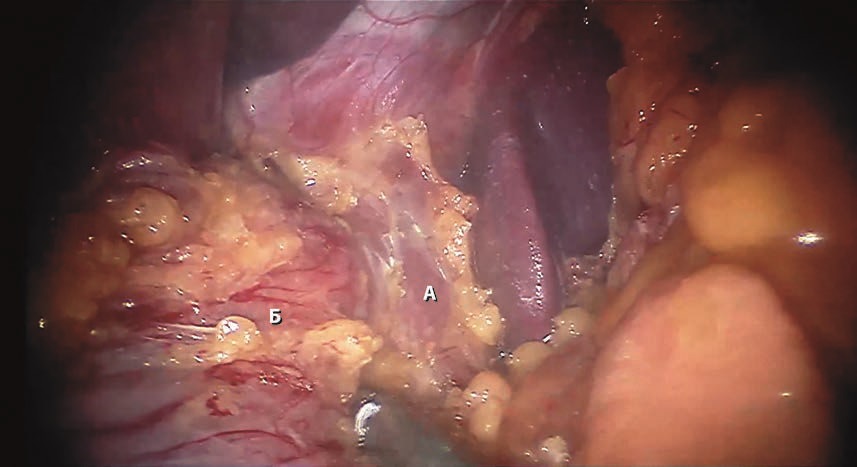 Рис. 4. Мобилизация желудка в области пищеводно-желудочного перехода.
Рис. 4. Мобилизация желудка в области пищеводно-желудочного перехода.
А — левая диафрагмальная ножка; Б — пищеводно-желудочный переход.
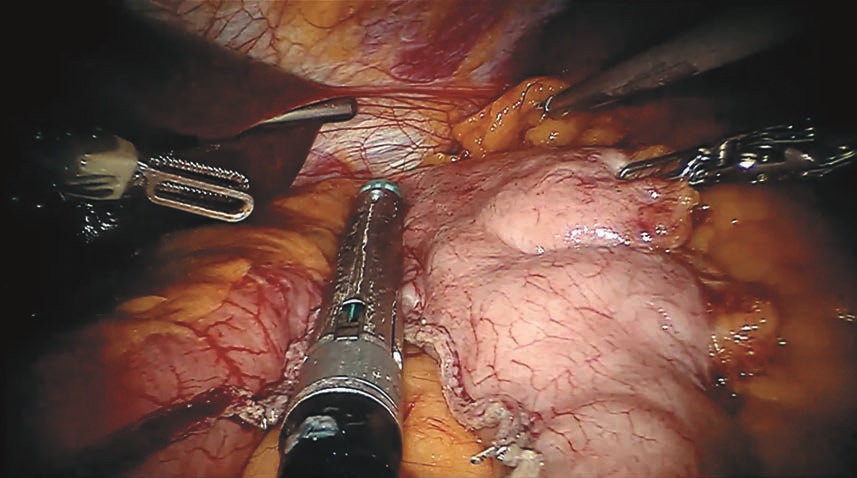 Рис. 5. Этап пересечения желудка с помощью линейного степлера. Интраоперационная фотография.
Рис. 5. Этап пересечения желудка с помощью линейного степлера. Интраоперационная фотография.
Послеоперационный период
На 1-е сутки после операции пациентам выполняли рентгенологическое исследование пассажа по желудочно-кишечному тракту с использованием водорастворимого контрастного препарата (рис. 7), удаление страховочного дренажа и затем разрешали прием жидкой пищи через рот по мере переносимости. Выписка происходила на 3-и сутки.
До выписки пациенты получали инфузионную терапию из расчета 15—20 мл/кг, фраксипарин 0,6 мл п/к вечером и ежедневно рабепразол 40 мг, сначала внутривенно, а затем перорально, в зависимости от переносимости. Прием рабепразола продолжался в течение минимум 1 мес после операции. В 1-й месяц после операции пациенты придерживались жидкой диеты, во 2-й — принимали блендерированную пищу, в 3-й — переходили на пюреобразную диету в течение еще 2 нед. Привычную пациентам диету с нормальной консистенцией разрешали через 3 мес после операции.
Исходные переменные
Дооперационные переменные включали демографические характеристики пациента (возраст, пол, рост, вес и ИМТ).
Интраоперационные переменные включали операционное время (время от хирургического разреза до успешной установки робота и общее оперативное время от разреза до закрытия кожи), кровопотерю >200 мл и симультанность вмешательства (например, иссечение кисты левой почки, интраоперационное ультразвуковое исследование (УЗИ), эзофагогастродуоденоскопия (ЭГДС)).
Послеоперационные переменные заключались в длительности госпитализации и наличии после операционных осложнений. Пациентов осматривали ежедневно во время пребывания в больнице и через 1, 3 и 6 мес после операции. Послеоперационное наблюдение включало оценку массы тела (кг) и любые осложнения.
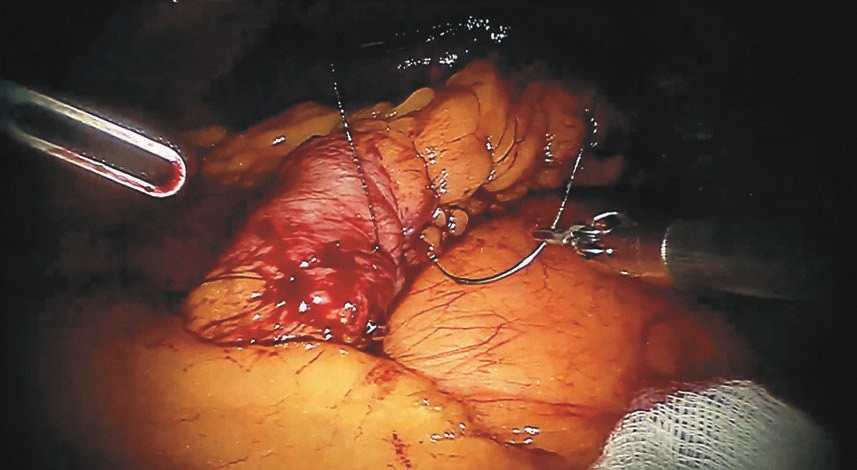 Рис. 6. Ушивание линии степлерного шва желудка. Интраоперационная фотография.
Рис. 6. Ушивание линии степлерного шва желудка. Интраоперационная фотография.
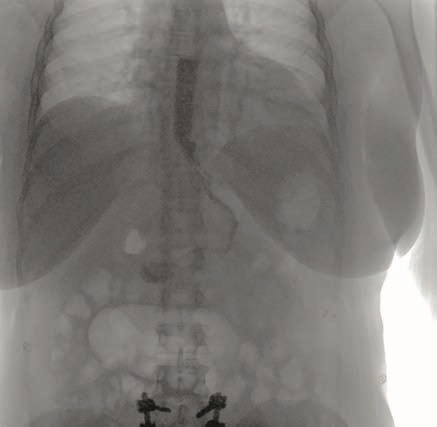 Рис. 7. Рентгенограмма желудка с водорастворимым контрастом после операции.
Рис. 7. Рентгенограмма желудка с водорастворимым контрастом после операции.
Статиститический анализ
Описательная статистика рассчитывалась с помощью программного обеспечения SPSS 23.0 («IBM», США). Данные в окончательном варианте представляли как медиану и персентили — Me [25%; 75%].
Результаты
Среди пациентов было 7 мужчин и 8 женщин. Средний возраст составил 50 [42,5; 56] лет, средний ИМТ — 42 [39,4; 44,6] кг/м2. Интраоперационных кровотечений (>200 мл) и периоперационных осложнений не было. В таблице представлены ИМТ и время операции, а также все дополнительные процедуры, выполненные в каждом случае.
Операционное время
Медиана общего операционного времени составила 194 [173,5; 241] мин, а медиана времени от разреза до стыковки — 35 [30; 36] мин. Причины задержки времени от разреза до стыковки робота включали: недостаточное пространство в операционном поле, внешние столкновения роботизированных манипуляторов на начальных этапах освоения техники, трудности с позиционированием роботизированных манипуляторов над туловищем пациента с ИМТ 50 кг/м2. Самое малое время, достигнутое при стыковке, составило 25 мин.
Данные оперированных пациентов
| Пациент | ИМТ (кг/м2) | Дополнительная операция | Время стыковки («докинг») | Время операции, мин |
| 1 | 41,0 | Нет | 45 | 245 |
| 2 | 35,7 | Иссечение кисты левой почки | 40 | 268 |
| 3 | 39,9 | Нет | 37 | 275 |
| 4 | 44,1 | Нет | 30 | 237 |
| 5 | 50,4 | УЗИ ЖП | 35 | 246 |
| 6 | 39,0 | Нет | 35 | 141 |
| 7 | 43,4 | ЭГДС | 28 | 196 |
| 8 | 34,6 | Нет | 32 | 148 |
| 9 | 42,0 | Нет | 40 | 165 |
| 10 | 41,9 | Нет | 30 | 193 |
| 11 | 44,7 | Нет | 25 | 195 |
| 12 | 50,8 | Нет | 35 | 194 |
| 13 | 54,9 | Предбрюшинная пластика пупочной грыжи (TAPP) | 35 | 185 |
| 14 | 44,4 | Нет | 35 | 182 |
| 15 | 33,5 | Нет | 25 | 124 |
Примечание. ЖП — желчный пузырь; TAPP — transabdominal preperitoneal — трансабдоминальный преперитонеальный доступ/пластика.
Послеоперационный период
Продолжительность пребывания в стационаре составила 3 койко-дня. Медиана потери избыточного веса, достигнутая через 6 мес, составила 37,55% [29,5; 51,2] с абсолютной медианой потери веса 19,5 [17; 21,75] кг.
Обоснование
Безопасное выполнение роботизированной «рукавной гастрэктомии» достижимо при работе команды на роботизированной платформе. Это первый российский опыт серии роботизированных операций в бариатрической хирургии. Меры безопасности, принятые перед началом операции, включали наличие у хирурга предыдущего лапароскопического опыта, предварительное обучение роботической технике, использование постоянной команды хирургов и обеспечение грамотной организации, проведения и контроля за ходом вмешательства («супервайзинг») для первых трех операций.
«Рукавная гастрэктомия» может быть выполнена безопасным роботизированным способом до более сложных бариатрических процедур, таких как желудочное шунтирование Roux-en-Y, в которых преимущество использования робота перед стандартной лапароскопией может быть более очевидным [8].
В последнее время в ряде бариатрических центров наблюдается интерес к созданию методологии и преодолению кривой обучения, связанной с технологией. Актуальность применения роботизированной технологии в повседневной практике недавно была подчеркнута в исследовании B. Ecker и соавт. [10], которое показало, что роботизированные процедуры «рукавной гастрэктомии» могут даже безопасно использоваться в качестве учебных процедур при подготовке хирургов для ознакомления стажеров с платформой. В настоящей серии были подробно описаны первые 15 случаев. Данные других групп показывают, что такое количество случаев относится к фазе активного обучения процедуре [9, 15], при этом для достижения привычного уровня навыков требуется 25 операций [16]. Кривая обучения времени установки роботизированной системы включает в себя всю команду хирургов. Следовательно, состав и слаженность работы команды очень важны [9]. Медиана оперативного времени для первых 15 последовательных роботических «рукавных гастрэктомий» составила 194 мин, что является разумным, если сравнивать с другими опубликованными сериями [8, 9, 17], в которых среднее оперативное время варьировало от 78 до 135 мин.
Отсутствие тактильной отдачи и кривая обучения, связанная с использованием робота, могут быть связаны с увеличением количества висцеральных травм при роботизированных операциях [18, 19]. Поэтому результаты нашей короткой серии обнадеживают, так как показывают, что приемлемое оперативное время и хорошие послеоперационные результаты достижимы даже на ранней стадии обучения. Роботизированная «рукавная гастрэктомия» стоит дороже (в данном исследовании проблему стоимости не изучали) и занимает больше времени, чем лапароскопическая процедура, хотя имеет схожие результаты [8, 16, 20]. Более вероятно, что при использовании робота для желудочного шунтирования Roux-en-Y будет достигнута выгода по времени и стоимости, особенно учитывая сокращение кривой обучения для этой процедуры при выполнении на роботизированной платформе [21].
Похожие меры безопасности были описаны при создании программы роботизированной колоректальной хирургии в Австралии, описанной S. Bell и соавт. [22], хотя используемые прокторы (сотрудники, осуществляющие контроль за прохожденим задания или теста) не были специализированы. Роль проктора заключается в информировании администрации о том, достаточна ли компетентность хирурга для получения временных привилегий на постоянное использование робота. Проктор дает некоторые пассивные инструкции, хотя ответственность перед пациентом остается за операционной бригадой. Проведение прокторинга первых случаев считается контрольной точкой безопасности при внедрении новых методик [23].
В качестве симультанных вмешательств проводили разделение спаек как лапароскопически, так и роботизированно. Также было выполнено иссечение кисты левой почки, представляющей собой другой квадрант для роботизированной хирургии, что было возможно в рамках данной роботизированной установки. Оперативное время в этих случаях было более длительным без дополнительных осложнений. Во время одной из операций была проведена интраоперационная гастроскопия для проверки целостности скрепочной линии. Несмотря на то что размещение портов может несколько отличаться, роботизированная установка для «рукавной гастрэктомии» будет применима и для других роботизированных операций. Краткосрочные результаты снижения веса обеспечивают доказательства, сопоставимые с результатами 6-месячной потери веса, полученными в сериях лапароскопических «рукавных гастрэктомий» [16, 20]. Мы ожидаем долгосрочных данных о результатах снижения веса.
Заключение
Таким образом, в доступной литературе нам не удалось найти подобный опыт внедрения роботизированной хирургии в бариатрическую практику в России. Выбранный подход был направлен на обеспечение безопасного перехода на новую технологию, чтобы подготовить бариатрическую бригаду к более сложным в будущем оперативным вмешательствам.
Участие авторов: Концепция и дизайн исследования — Выборный М.И., Колыгин А.В.
Сбор и обработка материала — Выборный М.И., Петров Д.И., Большаков Г.В.
Статистическая обработка — Петров Д.И.
Написание текста — Петров Д.И.
Редактирование — Выборный М.И., Колыгин А.В., Большаков Г.В
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.