Робот-ассистированная резекция кисты холедоха у ребенка
Резюме
Общепринятым методом лечения кист холедоха является полное удаление кистозно-измененных внепеченочных желчных протоков и желчного пузыря с наложением билиодигестивного анастомоза. В последнее время минимально инвазивные вмешательства становятся золотым стандартом в гепатобилиарной хирургии детского возраста. Однако при всех очевидных преимуществах лапароскопическая резекция кист холедоха имеет ряд недостатков, связанных с затруднением позиционирования инструментов в условиях ограниченного пространства. Недостатки лапароскопии могут быть компенсированы применением хирургических роботов. Девочке, 13 лет, выполнены робот-ассистированная резекция кисты гепатикохоледоха, холецистэктомия, гепатикоеюностомия с выключенной по Ру петлей тонкой кишки. Общее время общей анестезии составило 6 ч, лапароскопический этап — 55 мин, докинг роботического комплекса — 35 мин, роботический этап операции — 230 мин, извлечение препарата и ушивание ран — 35 мин. Послеоперационный период гладкий, энтеральная нагрузка начата на 3-и сутки, дренаж удален на 5-е сутки, выписана из стационара на 10-е сутки. Катамнез прослежен в течение 6 мес, состояние удовлетворительное. Таким образом, выполнение робот-асситированных резекций кист холе- доха у детей возможно и безопасно.
Введение
Врожденное кистозное расширение общего желчно- го протока (киста холедоха) — редкий порок развития, который может сопровождаться холангитом, панкреатитом, приводить к образованию желчных камней и возникновению холангиокарциномы [1, 2]. Частота встречаемости порока колеблется от 1 случая на 100 000 человек до 1 случая на 150 000 человек в европейских странах и 1 случая на 13 000 человек в Азии [2—4]. В настоящее время общепринятым методом лечения кист холедоха является полное удаление кистозно измененных внепеченочных желчных протоков и желчного пузыря с наложением билио- дигестивного анастомоза [5]. С 1990-х годов для выполнения этих операций у детей стали применять лапароскопический доступ, популярность которого прогрессивно увеличивалась параллельно широкому внедрению лапароскопии в педиатрическую практику [6, 7]. Однако наложение гепатикоеюноанастомоза в ходе лапароскопического вмешательства требует от хирурга высокой квалификации и большого опыта. Недостатки лапароскопии, связанные со сложностью наложения интракорпоральных швов и формированием узлов, могут быть компенсированы применением хирургического робота [8]. С момента первого сообщения Woo и со- авт. о роботической экстирпации кисты холедоха у ребенка в 2006 г. данный метод получил широкое распространение в мировой детской хирургии [9]. Представляем свой первый опыт роботической операции у ребенка с кистой холедоха.
Клиническое наблюдение
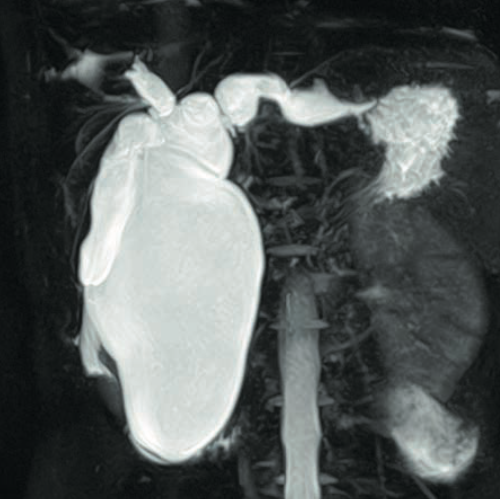
Девочка Э., 13 лет, госпитализирована с жалобами на периодическую в течение года ноющую боль в верхних отделах живота. Рост 158 см, масса тела 40 кг, индекс массы тела 16 кг/м2, дефицит массы тела. При осмотре и пальпации живота отмечается болезненность в правом подреберье, слабоположительные пузырные симптомы, край печени выступает из-под реберной дуги на 1,5 см, закруглен. В лабораторных и биохимических анализах значимых от клонений от нормы не выявлено. По данным УЗИ в воротах печени определяется кистозное образова- ние размером 150×75×70 мм, объемом около 380 мл с толщиной стенки до 3,5 мм. Внутрипеченочные желчевыводящие протоки расширены: левый долевой проток до 9 мм, правый — до 22 мм. Желчный пузырь размером 60×28 мм, стенка уплотнена, просвет гомогенный. По данным магнитно-резонансной холангиопанкреатографии: общий желчный проток кистозно изменен, размером 150×82×74 мм, левый печеночный проток неравномерно расширен до 18—22 мм до уровня сегментарных протоков, правый печеночный проток расширен до 9 мм (рис. 1). Желчный пузырь размером 70×28 мм, вытянутой формы с множественными перетяжками. На основании данных лучевых методов выставлен диагноз: киста общего желчного протока VIa типа (по T. Todani и соавт., 1977) [10, 11].
Выполнены робот-ассистированная резекция кисты гепатикохоледоха, холецистэктомия, гепатикоеюностомия с выключенной по Ру петлей тонкой кишки, дренирование подпеченочного пространства.
Под комбинированной эндотрахеальной общей анестезией в положении больной на спине (с подложенным под грудную клетку до XII ребра валиком высотой около 10 см под пупком) открытым способом введен троакар 12 мм, наложен карбоксиперитонеум 14 мм рт.ст., введена 5-миллиметровая 30о лапароскопическая оптика. Рабочие троакары 5 мм введены справа и слева от пупка. Начальный участок тощей кишки экстрапериотонизирован через дугообразно расширенный околопупочный троакарный доступ. В 20 см от связки Трейтца тощая кишка пересечена аппаратом Echelon flex 60. В 35 см аборальнее 60 наложен межкишечный анастомоз по типу бок в бок с помощью аппарата Echelon flex. Места введения бранш аппарата ушиты обвивным швом нитями vicryl 4/0. Тонкая кишка с анастомозом погружена в брюшную полость. Рана в околопупочной области ушита до оптического порта 12 мм. Троакары 5 мм заменены на роботические порты 8 мм. В правой люмбодорзальной области установлен дополнительный роботический порт 8 мм. В левую подвздошную область установлен троакар 5 мм для лапароскопической ассистенции. Введены рабочие инструменты робот-ассистированной хирургической системы da Vinci Surgical System (рис. 2).
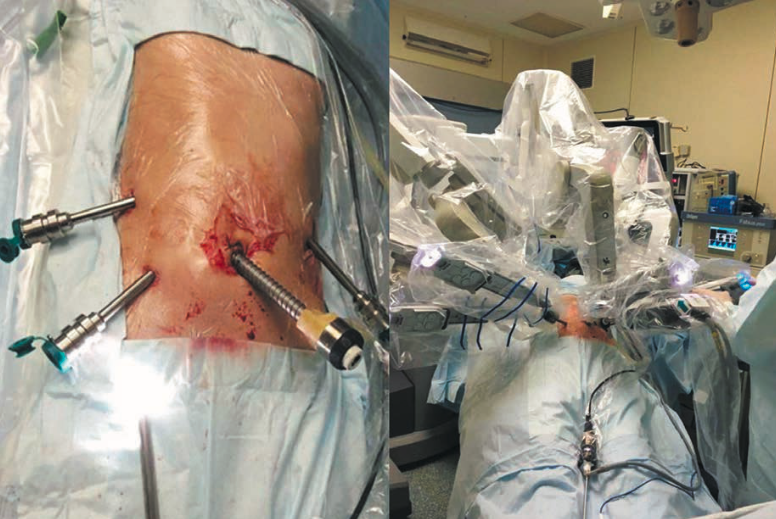 Рис. 2. Интраоперационные фотографии этапов установки троакаров для роботических инструментов. Fig. 2. Intraoperative docking of robotic system.
Рис. 2. Интраоперационные фотографии этапов установки троакаров для роботических инструментов. Fig. 2. Intraoperative docking of robotic system.
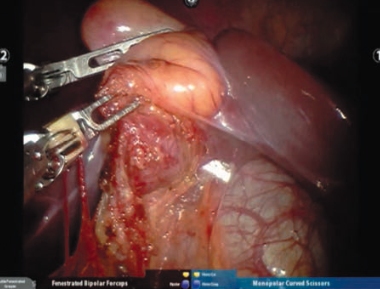 Рис. 3. Интраоперационная фотография кисты гепатикохоледоха. Fig. 3. Intraoperative image of hepaticocholedochal cyst.
Рис. 3. Интраоперационная фотография кисты гепатикохоледоха. Fig. 3. Intraoperative image of hepaticocholedochal cyst.
При ревизии выявляется напряженная киста гепатикохоледоха диаметром до 15 см (рис. 3). Желчный пузырь в области шейки имеет S-образный изгиб, фиксированнный к поперечно-ободочной кишке в области шейки. Кистозно измененный гепатикохоледох отделен от элементов гепатодуоденальной связки и головки поджелудочной железы. Киста вскрыта, удалено до 500 мл темной желчи. Желчный пузырь отделен от ложа. Общий печеночный проток пересечен на 1 см ниже бифуркации, диаметр его на этом уровне около 2 см. Сформированная ранее Ру-петля проведена позадиободочно к воротам печени. После вскрытия просвета кишки по противобрыжеечному краю наложен гепатикоеюноанастомоз по типу конец в бок однорядным обвивным швом нитями vicryl 4/0 (рис. 4). Брюшная полость осушена. Через латеральный порт справа дренировано подпеченочное пространство. Иссеченная киста и желчный пузырь удалены через околопупочный троакарный доступ. Общее время анестезиологического пособия 6 ч. Позиционирование больного, стыковка лапароскопической стойки и формирование Ру-петли выполнено за 55 мин. Введение роботических троакаров, стыковка роботического комплекса заняли 35 мин. Роботический этап операции составил 230 мин. На извлечение препарата и ушивание троакарных ран ушло 35 мин. Общий объем интраоперационной кровопотери 100 мл. Послеоперационный период протекал без особенностей. Энтеральная нагрузка начата на 3-и сутки. Дренаж удален на 5-е сутки. Выписана из стационара на 10-е сутки. Катамнез прослежен в течение 6 мес. Состояние удовлетворительное, жалоб не предъявляет. По данным УЗИ отмечено уменьшение диаметра левого долевого печеночного протока до 2,5 мм, правого долевого печеночного протока до 4,6 мм.
Обсуждение
Киста холедоха является относительно редким пороком развития. В большинстве наблюдений кисты холедоха выявляют и оперируют в детском возрасте. Кисты холедоха могут проявлять себя триадой симптомов: болью в животе, желтухой, объемным образованием в правом подреберье, однако классическая триада присутствует только в 40% случаев. С возрастом у таких больных все чаще появляются симптомы рецидивирующего панкреатита и холедохолитиаза [12]. При гистологическом исследовании стенок кистозно измененного холедоха зачастую отмечается полное отсутствие мышечной пластинки или хаотичное расположение гладкомышечных клеток, что указывает на невозможность полноценного выполнения функции транспорта желчи. Как следствие, возникает истончение стенки желчных протоков с возможной их спонтанной перфорацией, которая отмечена в 1% клинических наблюдений [13].
При кистах холедоха в 70% случаев наблюдают так называемое аномальное панкреатикобилиарное соустье, при котором область слияния общего желчного и панкреатического протоков располагается за пределами стенки двенадцатиперстной кишки и сфинктера Одди. Данный анатомический вариант способствует беспрепятственному рефлюксу панкреатического секрета в полость кисты холедоха с развитием хронического воспаления и почти полной утратой эпителиальной выстилки желчных протоков, а также возможной метаплазией билиарного эпителия, что в конечном счете может привести к возникновению холангиокарциномы [14].
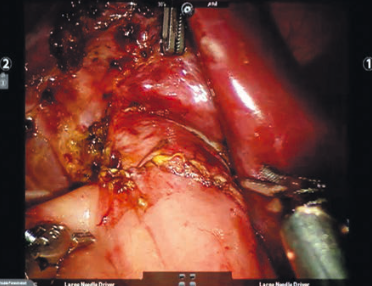 Рис. 4. Интраоперационная фотография гепатикоеюноанастомоза по типу конец в бок. Fig. 4. Intraoperative image of end-to-side hepaticojejunostomy.
Рис. 4. Интраоперационная фотография гепатикоеюноанастомоза по типу конец в бок. Fig. 4. Intraoperative image of end-to-side hepaticojejunostomy.
Общепринятая классификация кистозных расширений желчных предложена F. Alonso-Lej и соавт. и модифицирова T. Todani и соавт. в 1977 г. [10, 11]. В нашем случае с учетом данных лучевых методов исследования у ребенка была киста общего желчного протока с вовлечением долевых протоков IVa типа. Факт установления диагноза кисты холедоха признается всеми абсолютным показанием к хирургическому лечению в любом возрасте. Объем радикального хирургического вмешательства у больных с кистами холедоха предполагает удаление кистозно измененных внепеченочных желчных протоков с холецистэктомией и наложением билиодигестивного анастомоза: гепатикоеюностомии на отключенной по Ру петле либо гепатикодуоденостомии [14]. Резекция кисты холедоха вследствие сложной анатомии порока развития желчных протоков традиционно рассматривалась у детей как открытая операция. В то же время увеличение в последние годы количества публикаций об успешном применении лапароскопических технологий, в том числе систематических обзоров и метаанализов, свидетельствует о том, что минимально инвазивные вмешательства становятся новым золотым стандартом в гепатобилиарной хирургии детского возраста [7, 15]. При всех очевидных преимуществах у лапароскопической резекции кист холедоха есть ряд недостатков, связанных с ограничением позиционирования инструментов при наложении анастомозов и формирования узлов в условиях ограниченного пространства. В ряде исследований, посвященных лапароскопическим реконструктивным операциям, указано на длительные кривые обучения хирургов [16]. Сохранить преимущества лапароскопии, такие как визуализация высокого разрешения, малотравматичность оперативного доступа, снижение риска инфицирования и пр., призваны хирургические роботы, чьи инструменты с широкой осью вращения бранш облегчают и ускоряют выполнение технически сложных этапов хирургических вмешательств [8].
Эволюция хирургических роботов и накопление опыта робот-ассистированных операций у детей позволили применить эту технику и в лечении кист холедоха. Так, первое сообщение успешной резекции кисты холедоха у ребенка опубликовано в 2006 г. [9]. С этого времени наблюдается увеличение числа центров, которые выполняют такие роботические операции. По данным литературы, к настоящему времени в мире выполнено более 100 роботических резекций кист холедоха у детей, и даже опубликованы данные о 60 подобных операциях [17]. Мы располагаем хирургической робот-асситированной системой da Vinci Surgical System Si III поко- ления (Intuitive Surgery Inc.), которую сегодня широко используют в мире. Система Da Vinci имеет 3D-систему визуализации высокой четкости и 10-кратного увеличения. Пульт управления оснащен моделирующим запястьем с функцией фильтрации встряхивания и подавления тремора, механические руки робота обладают большим диапазоном действий, чем традиционные лапароскопические инструменты. Технические особенности робота делают процесс диссекции тканей и формирования анастомозов более простым и безопасным.
Резекция кисты холедоха с применением робота является технически сложной операцией, это связано с тем, что объем брюшной полости у ребенка мал, широкий обзор операционного поля ограничен, а расстояние между билиодигестивным и межкишечным анастомозом велико. Поэтому оперирующему хирургу предстоит решить несколько сложных технических моментов. Одним из них является формирование межкишечного анастомоза. При формировании отключенной петли тонкой кишки по Ру существует 2 подхода к наложению межкишечного анастомоза: интракорпоральный и экстракорпоральный. Мы выполнили этот этап экстракорпорально с применением стандартной лапароскопии до подключения роботической системы. Тонкая кишка экстрапериотонизирована через дугообразно расширенный подпупочный доступ, формирование Ру-петли проведено при помощи сшивающих аппаратов. Данный подход является наиболее популярным из описанных в литературе [8, 18].
Другой проблемой является доступ к воротам печени. Для облегчения доступа к воротам печени существует ряд хирургических приемов: применение тракционных швов с фиксацией круглой связки печени и/или прошиванием желчного пузыря к передней брюшной стенке, использование ретрактора печени, введение дополнительных троакаров, через которые ассистент обеспечивает отведение печени, а также использование 3-й роботической «руки» [8, 18, 19]. При роботических операциях, если размер ребенка позволяет установить 3-й роботический троакар без конфликта «рук» робота (минимальное расстояние между троакарами 8 см), предпочтительно использовать именно его, что значительно облегчает диссекцию и формирование анастомозов. Помимо этого, на роботическом этапе мы использовали 3-ю «руку», которую в неактивном режиме использовали для отведения печени, при активации она участвовала в тракции кисты и формировании анастомоза.
Спорным аспектом внедрения роботических операций является общее время анестезии, которое на начальном этапе, как правило, больше, чем при открытых и лапароскопических операциях. Так, среднее время робот- ассистированного удаление кист холедоха, по данным различных публикаций, составляет 180—520 мин [8, 18, 19]. Важно отметить, что сокращение времени операции обеспечивается не только за счет совершенствования навыков роботических манипуляций, но и за счет более быстрого позиционирования стола и пациента и стыковки (docking) робота, что зависит от слаженной работы всей операционной бригады и в опытных коллективах занимает не более 10—15 мин. В нашем случае мы затратили на докинг и обратный докинг 50 мин (35 и 15 мин соответственно), что сопоставимо с данными, представленными в [20, 21]. Распространению роботической хирургии препятствует высокая стоимость оборудования и инструментов. В связи с этим внедрение роботических операций в педиатрическую практику происходит медленно. Так, даже в США в большинстве детских больниц до 2015 г. не было собственных роботических установок и использовалось оборудование взрослых стационаров [22]. Подобная ситуация сейчас наблюдается и в России, где появляются сообщения о роботических операций детям в клиниках, имеющих как взрослые, так и детские стационары [23, 24].
Заключение
Выполнение робот-асситированных резекций кист холедоха у детей возможно и безопасно. Данные операции следует выполнять в центрах с соответствующим техническим оснащением коллективами детских хирургов с большим опытом открытых и лапароскопических операций на органах гепатобилиарной зоны.
Авторы заявляют об отсутствии конфликта интересов. The authors declare no conflicts of interest.






