Особенности обучения лапароскопической резекции печени после первоначального освоения робот-ассистированной технологии
Цель. Оценить кривую обучения лапароскопическим резекциям печени хирурга, имеющего опыт робот-ассистированных резекций печени, при помощи метода CUSUM.
Материал и методы. Ретроспективно анализировали результаты лапароскопических резекций печени по поводу злокачественных и доброкачественных новообразований, выполненных с 2015 г. по декабрь 2020 г., и роботассистированных резекций печени с 2010 по 2020 г. Оценивали кривую обучения лапароскопическим резекциям печени хирурга, освоившего робот-ассистированные резекции большой сложности. При выборе границ между периодами обучения в соответствии с полученными графиками CUSUM ориентировались на критические изменения индекса сложности резекции (IWATE и IMM), продолжительности операции, кровопотери, частоты послеоперационных осложнений. Проведено сравнение основных периоперационных событий между группами лапароскопических и робот-ассистированных резекций в каждом из периодов обучения.
Результаты. Выполнено 174 лапароскопических и 57 робот-ассистированных резекций печени. Продолжительность 1-го периода обучения составила 11 робот-ассистированных резекций и 20 лапароскопических, 2-го периода – 16 и 20, 3-го периода – 30 и 134. Во 2-м периоде достоверно увеличился индекс сложности резекции для обеих групп, при этом объем кровопотери, число послеоперационных осложнений и продолжительность госпитального лечения достоверно не различались. Во 2-м периоде обучения в обеих группах время оперативного вмешательства было достоверно больше.
Заключение. Изучение динамики сложности операции с использованием метода CUSUM является надежным, контролируемым способом оценки кривой обучения резекции печени. Первоначальное прохождение кривой обучения робот-ассистированным резекциям печени сокращает длительность кривой обучения лапароскопическим резекциям по сравнению с опубликованными данными других авторов.
Введение
Преимущества лапароскопических резекций печени (ЛРП) были показаны во многих сравнительных исследованиях [1, 2]. В последние годы растет число публикаций , посвященных оценке кривой обучения (КО) минимально инва зивным резекциям печени (РП) [3–5]. В последнее десятилетие для оценки КО в медицине используют метод кумулятивных сумм (CUSUM) [3]. Отдельный интерес представляет анализ КО с точки зрения ее “привязки” к динамике сложности ЛРП в отличие от КО лапароскопическим резекциям других органов, в анализе которой чаще основываются на частоте конверсии и других показателях (кровопотеря, длительность операции и др.) [6–11]. В литературе нет исследований, направленных на изучение влияния опыта робот-ассистированных РП (РАРП) на КО ЛРП.
Цель исследования – оценить кривую обучения лапароскопическим резекциям печени хирурга, имеющего опыт робот-ассистированных резекций, при помощи метода CUSUM.
Материал и методы
Исследование основано на ретроспективном изучении результатов лечения пациентов, перенесших ЛРП, которые были зарегистрированы в проспективной базе данных. Основные критерии включения пациентов: анатомическая или атипичная РП по поводу злокачественной опухоли (метастазы колоректального и неколоректального рака, гепатоцеллюлярная карцинома, внутрипеченочная холангиокарцинома, рак желчного пузыря), доброкачественных заболеваний (фокальная нодулярная гиперплазия, гемангиома, аденома, цистаденома, абсцесс печени, внутрипеченочный холангиолитиаз), а также при паразитарных поражениях (альвеококкоз, эхинококкоз). Пациентов с эхинококкозом включали в исследование, если им была выполнена тотальная или субтотальная перицистэктомия. Исключали пациентов, которым выполнили фенестрацию простых кист печени или частичную перицистэктомию при эхинококкозе.
Индекс сложности резекции печени был рассчитан по шкалам IWATE [12] и IMM [13]. Первичной конечной точкой исследования было определение продолжительности периодов обучения методу ЛРП и РАРП. Для этого был использован метод кумулятивных сумм (CUSUM), в котором, согласно принятой ранее методологии, определяли три периода: 1-й, или начальный, 2-й, или период расширения показаний, и 3-й, или период плато [14]. Вторичными точками исследования были сравнение периодов обучения согласно результатам хирургического лечения: продолжительности резекции, объему кровопотери, частоте осложнений и срокам пребывания пациентов в стационаре после операции. Послеоперационные осложнения оценивали в соответствии с классификацией Clavien– Dindo (CD). Все операции были выполнены одним хирургом. К началу выполнения ЛРП хирург уже прошел КО РАРП.
При статистической обработке непрерывные данные, представленные как медианные значения, сравнивали с помощью теста Краскела– Уоллиса, ANOVA. Критерий χ2 Пирсона использовали для сравнения категориальных переменных. Значение р < 0,05 считали статистически значимым. Для анализа данных был применен программный пакет Statistica (V.12, StatSoft).
Результаты
Анализировали результаты резекции печени у 231 пациента: 174 больным выполнена ЛРП, 57 – РАРП (табл. 1). В группе РАРП было достоверно больше пациентов с доброкачественными новообразованиями печени. Возраст пациентов, частота злокачественных опухолей и частота абдо минальных оперативных вмешательств в анамнезе были достоверно меньше по сравнению с группой ЛРП. Распределение ЛРП и РАРП по числу и топографии резецированных сегментов представлено в табл. 2. В группе РАРП чаще выполняли анатомическую резекцию как в отдельных топографических вариантах, так и в целом. Группы ЛРП и РАРП были сопоставимы как по индексу сложности, рассчитанному по двум шкалам, так и по 3 факторам из 4, учитываемых при расчете индекса сложности резекции одной из шкал (критерии IWATE; табл. 3).
Таблица 1. Характеристика пациентов
|
Параметр |
ЛРП |
РАРП |
p |
|
Число пациентов, абс. (%) всего женщин, мужчин с доброкачественными опухолями с паразитарными заболеваниями со злокачественными опухолями перенесших абдоминальные операции |
174 101, 73 47 (27) 20 (11,5) 107 (61,5) 71 (40,8) |
57 40, 17 30 (52,6) 5 (8,8) 22 (38,6) 12 (21) |
– 0,069 0,0004 0,383 0,001 0,003 |
| Возраст, лет |
56 (46–64) |
50 (38–62) |
0,011 |
Таблица 2. Распределение пациентов по объему операции
| Объем РП | Число наблюдений, абс. (%) | p | |
| ЛРП | РАРП | ||
|
Правосторонняя гемигепатэктомия Левосторонняя гемигепатэктомия Бисегментэктомия VI, VII Сегментэктомия VII, VIII, I, IVa Атипичная резекция сегментов I, IVa, VII, VIII Анатомическая резекция сегментов V, VI, II, III Атипичная резекция сегментов V, VI, II, III Всех анатомических резекций |
17 (10) 11 (6) 8 (5) 22 (13) 43 (25) 23 (13) 50 (29) 81 (47) |
3 (5) 2 (4) 8 (14) 7 (12) 10 (16) 16 (28) 11 (19) 36 (63) |
0,223 0,335 0,020 0,574 0,175 0,010 0,107 0,021 |
Таблица 3. Индекс сложности резекции и факторы, влияющие на него
|
Параметр |
ЛРП |
РАРП |
p |
|
Наблюдений близкой синтопии с крупными сосудами, абс. (%) Больных циррозом, абс. (%) Сегментэктомий VII, VIII, I, IVa, абс. (%) Размер опухоли, мм Индекс сложности РП по IWATE, баллы Индекс сложности РП по IMM, баллы |
59 (33,9) 17 (9,8) 22 (12,6) 65 (15–250) 6 (1–11) 4,6 (1–10) |
27 (47) 8 (14) 7 (12,3) 70 (17–142) 7 (2–11) 4,7 (1–7) |
0,024 0,255 0,574 0,223 0,216 0,669 |
При помощи метода CUSUM построены диаграммы изменения индекса сложности РП и основных результатов РАРП и ЛРП (кровопотеря, длительность резекции, частота осложнений). Продолжительность периодов изначально оценивали по динамике сложности РП. Продолжительность 1-го, начального периода составила 11 РАРП и 20 ЛРП; в этот период выполняли преимущественно операции низкого уровня сложности по IWATE. Продолжительность 2-го периода составила 16 РАРП и 20 ЛРП; в этом периоде произошло расширение показаний к резекциям большего уровня сложности. Стабилизация – при отсутствии существенной динамики на диаграмме (плато) – произошла в 3-м периоде: 30 РАРП и 134 ЛРП (рис. 1 и 2).
При выборе границ между периодами обучения оценивали динамику кривой CUSUM. Наи более выраженные амплитудные колебания ее отражали принципиальную смену величины изучаемого показателя, что практически должно соответствовать смене периода обучения. Для подтверждения этой гипотезы рассмотрели изменение других объективных периоперационных показателей. В качестве контрольного показателя использована оценка сложности, рассчитанная с помощью других критериев (шкала IММ). Динамика сложности РАРП и ЛРП по шкале IMM представлена на рис. 3 и 4. Противоречий с динамикой сложности по критериям IWATE не отмечено, что подтвердило продолжительность периодов обучения РАРП и ЛРП. В начальном периоде обучения диаграмма соответствовала минимальным значениям индекса сложности начальных 11 РАРП и 20 ЛРП. После 11-й и 20-й операции отмечен заметный подъем уровня сложности резекции, что означает переход во 2-й период КО за счет расширения показаний к РАРП (p = 0,002) и ЛРП (p = 0,020) (табл. 4, 5).
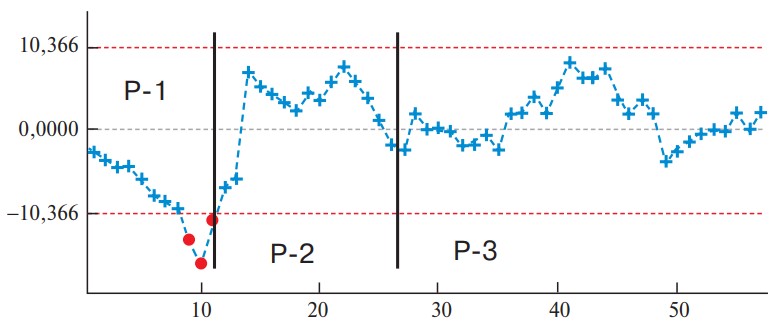 Рис. 1. Диаграмма. Изменение индекса сложности РАРП (IWATE). Здесьи далее: Р-1 – начальный
период; Р-2 – период расширения показаний; Р-3 – период стабилизации; по оси абсцисс – число
наблюдений.
Рис. 1. Диаграмма. Изменение индекса сложности РАРП (IWATE). Здесьи далее: Р-1 – начальный
период; Р-2 – период расширения показаний; Р-3 – период стабилизации; по оси абсцисс – число
наблюдений.
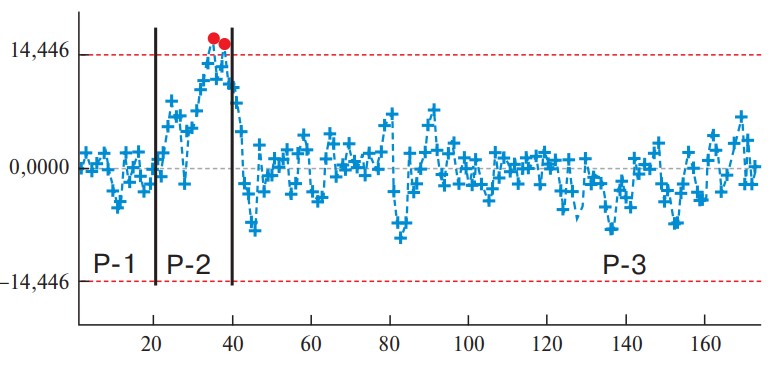
Рис. 2. Диаграмма. Изменение индекса сложности ЛРП (IWATE).
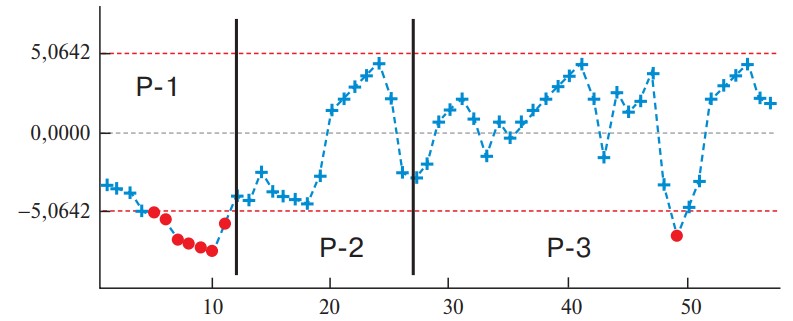
Рис. 3. Диаграмма. Изменение индекса сложности РАРП (IMM).
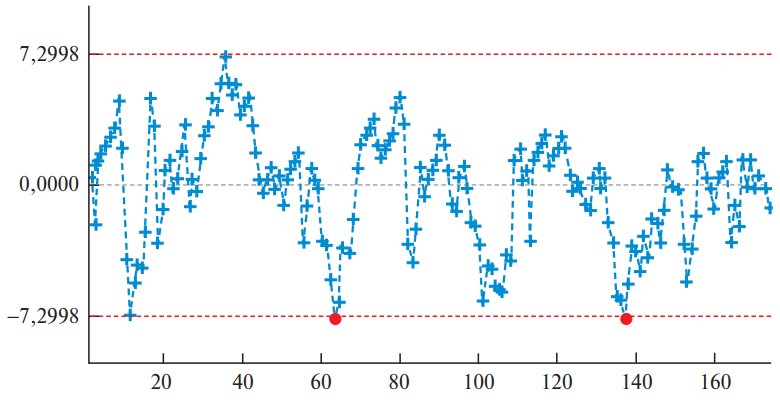
Рис. 4. Диаграмма. Изменение индекса сложности ЛРП (IMM).
Таблица 4. Сравнение индексов сложности и ближайших результатов РАРП
| Параметр | 1-й период | 2-й период | 3-й период | p |
|
Число наблюдений, абс. Индекс сложности РП IWATE, баллы Индекс сложности РП IMM, баллы Объем кровопотери, мл Время операции, мин Число конверсий, абс. Число осложнений, абс. Пребывание в стационаре после операции, сут |
11 5 (3–5) 4 (3–4) 200 (100–300) 310 (200–330) – 2 8 (8–13) |
16 7 (6–10) 5 (4–6) 230 (100–450) 420 (350–480) 2 4 10 (8–12) |
30 7 (6–10) 6 (4–6) 250 (100–400) 350 (275–450) 1 6 8 (7–10) |
– 0,002 0,093 0,545 0,026 0,341 0,527 0,812 |
После 27 РАРП и 40 ЛРП отмечена стабилизация показателей (переход в плато). Для подтверждения продолжительности периодов обучения, определенных по динамике сложности РП, построе ны диаграммы изменения периоперационных показателей – кровопотери, времени операции и частоты осложнений (рис. 5–7). Отмеченные изменения периоперационных пока зателей соответствуют продолжительности перио дов обучения РАРП. Аналогичные диаграммы для ЛРП представлены на рис. 8–10. Диаграммы CUSUM, построенные для периоперационных параметров ЛРП, продемонстрировали продолжительность периодов обучения, аналогичную рассчитанной по динамике сложности ЛРП. Дополнительным аргументом в пользу корректности рассчитанной продолжительности периодов обучения может служить величина различий изученных периоперационных параметров между периодами КО (см. табл. 4). Достоверные отличия между периодами выявлены в значениях индекса сложности операций по критериям IWATE и в длительности операции. Во 2-м периоде имел место рост объема кровопотери, но различия недостоверны. Сравнение периоперационных показателей ЛРП представлено в табл. 5.
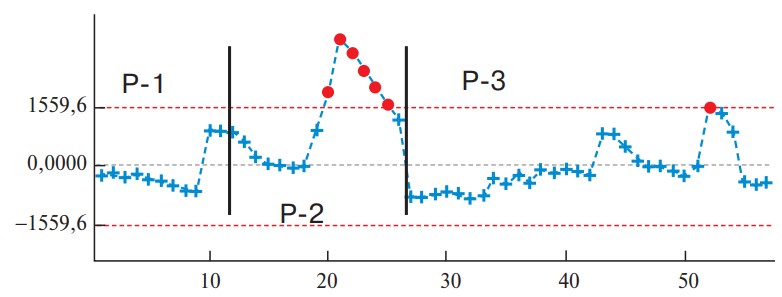
Рис. 5. Диаграмма. Изменение объема кровопотери при РАРП.
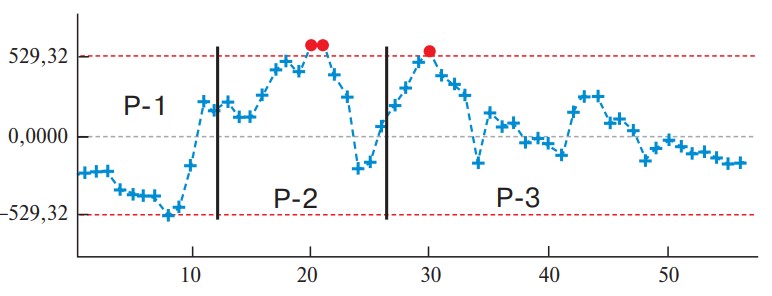
Рис. 6. Диаграмма. Изменение продолжительности РАРП.
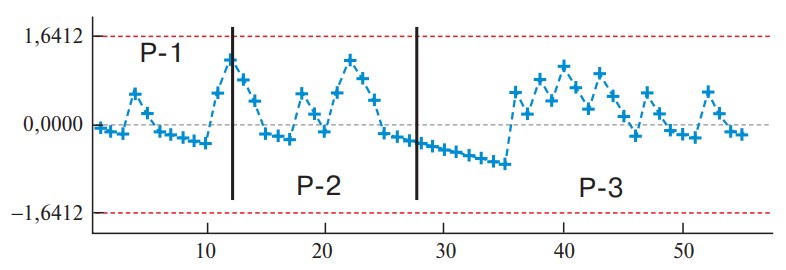
Рис. 7. Диаграмма. Изменение частоты осложнений после РАРП (CDII–V).
Таблица 5. Сравнение индексов сложности и ближайших результатов ЛРП
| Параметр | 1-й период | 2-й период | 3-й период | p |
|
Число наблюдений, абс. Индекс сложности РП IWATE, баллы Индекс сложности РП IMM, баллы Объем кровопотери, мл Время операции, мин Число конверсий, абс. Число осложнений, абс. Пребывание в стационаре после операции, сут |
20 6 (5–9) 6 (4–6) 200 (50–350) 310 (260–450) – 3 7 (6–10) |
20 9 (7–11) 6 (5–7) 300 (175–500) 460 (340–570) 5 4 8 (7–9) |
134 6 (4–11) 5 (4–6) 200 (100–300) 260 (200–370) 7 16 7 (5–9) |
– 0,020 0,291 0,183 0,048 0,027 0,521 0,213 |
Во 2-м периоде обучения ЛРП, так же как и РАРП, произошло достоверное увеличение индекса сложности РП по критериям IWATE и продолжительности операции. Важным обстоятельством, характеризующим накопление хирургических навыков, является отсутствие разли чий между периодами по величине кровопотери и частоте осложнений, несмотря на объективное увеличение сложности операций, с одной стороны, и увеличение продолжительности операции как показателя, отражающего процесс адаптации хирурга к новым, более сложным условиям, – с другой. В отличие от РАРП во 2-м периоде КО ЛРП увеличилась частота конверсий. Результаты сравнения периоперационных исходов косвенным образом подтверждают правильность расчетов продолжительности периодов КО для РАРП и ЛРП.
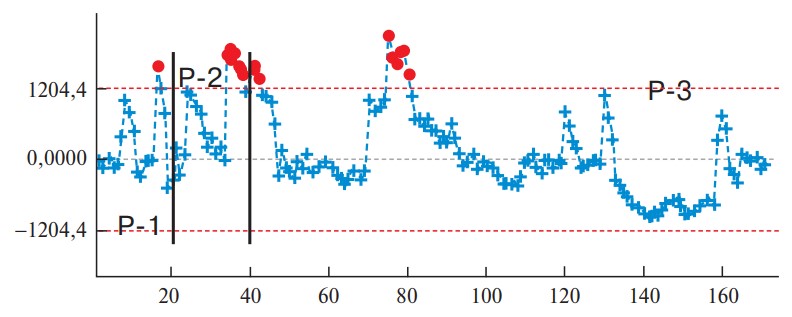
Рис. 8. Диаграмма. Изменение объема кровопотери при ЛРП.
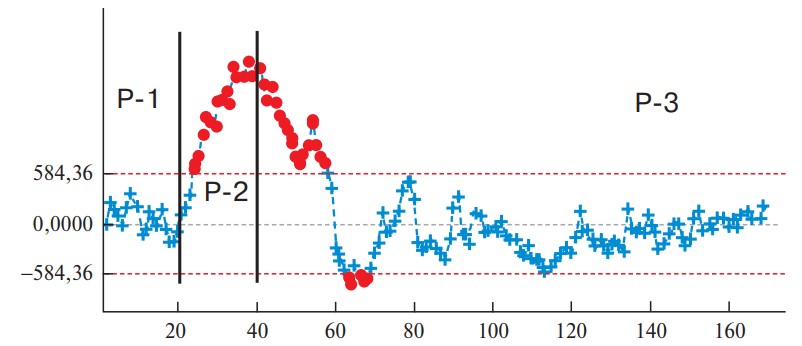
Рис. 9. Диаграмма. Изменение продолжительности ЛРП.
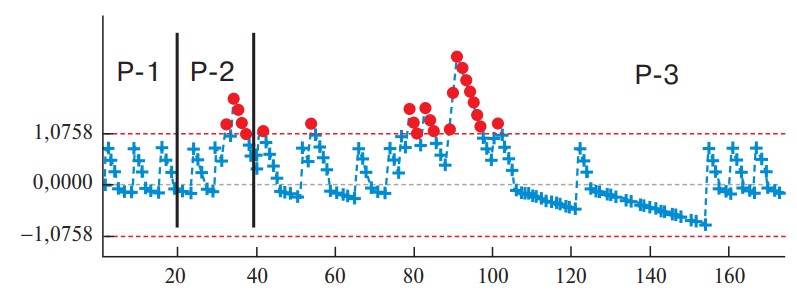
Риc. 10. Диаграмма. Изменение частоты осложнений после ЛРП (CD II–V).
Обсуждение
В первых публикациях, посвященных оценке КО ЛРП, в качестве основного критерия применяли частоту конверсий. В одной из публикаций авторы впервые сообщили о КО с помощью метода CUSUM [3]. Рассмотрев результаты 174 ЛРП за 12 лет, они пришли к выводу, что для достижения пороговой точки минимального коэффициента конверсии потребовалось 60 ЛРП. Другими словами, после 60 операций коэффициент конверсии достиг среднего значения для всей когорты и с этого момента только улучшался. При тщательном отборе пациентов и совершенствовании хирургических методов частота конверсии ЛРП постепенно уменьшалась [15–18]. В дальнейшем стало понятно, что коэффициент конверсии не является универсальным критерием оценки КО. Это послужило основанием для анализа других параметров, в частности интраоперационной кровопотери, длительности операций, частоты осложнений и др. [19]. На основании оценки динамики перечисленных показателей было установлено, что для обширных РП и резекций задних сегментов начальный этап освоения КО составил 60 операций [4]. Другими исследователями было показано, что для уменьшения частоты послеоперационных осложнений необходимо выполнить 60 малых резекций, что позволяет перейти к выполнению более сложных вмешательств [15].
Оценка результатов РП, равно как и обучение, в отличие от операций на других органах, сопряжена с необходимостью учитывать большее разнообразие вариантов операции в силу специфики хирургической анатомии печени. Разница в технологии и рисках некоторых вариантов РП столь существенна, что результаты этих операций, равно как и КО, фактически нельзя сравнивать. Выходом может быть сравнение КО однотипных операций, что и делает ряд авторов [4, 19]. Другим вариантом учета разнообразия условий выполнения ЛРП является разработка универсальной системы оценки технической сложности операции, что позволит унифицировать результаты сравнения, а также получить дополнительный способ количественной оценки КО за счет мониторинга скорости освоения более сложных ЛРП.
На 2-й Международной согласительной конференции по ЛРП (Мориока, Япония, 2014) G. Wakabayashi и соавт. предложили шкалу оценки сложности предполагаемой ЛРП (IWATE Criteria) [12]. Шкала предполагает 12-балльный индекс сложности на основе совокупной оценки нескольких факторов: расположение (сегменты) и размер опухоли, ее близость к крупным сосудам, вариант резекции (анатомическая или атипичная) и сохранность функции печени. Учитывается и объем резекции.
В последние годы в литературе появились отдельные публикации, оценивающие КО с позиции учета сложности ЛРП. Следует отметить различие подходов к учету этого показателя. В одном из исследований изучена КО для ЛРП малой сложности, которая составила 25–30 операций [20]. В другом исследовании КО ЛРП авторы использовали анализ CUSUM и установили, что для преодоления КО для конечных точек времени операции, конверсии и расчетной кровопотери потребовалось 160 резекций [21]. В литературе существуют противоречия в оценке продолжительности КО.
Представленное исследование является первым в оценке влияния опыта РАРП на КО ЛРП. Результаты исследования убедительно показывают такое влияние, поскольку продолжительность КО ЛРП была существенно короче (20 операций) по сравнению с данными других авторов. Объективность оценки продолжительности КО и ее отдельных периодов подтверждена совпадением результатов оценки по разным шкалам определения сложности РП и динамикой периоперационных показателей.
КО РАРП и ЛРП имели небезынтересные отличия. В группе РАРП, особенно на начальных периодах КО, преобладали пациенты с доброкачественными образованиями. Пациенты со злокачественными и паразитарными заболеваниями были оперированы только после прохождения 1-го периода КО. Преобладание в группе РАРП пациентов без перенесенных ранее хирургических вмешательств на брюшной полости можно объяснить отсутствием достаточного опыта минимально инвазивной хирургии печени, который был накоплен во время обучения РАРП и в дальнейшем при обучении ЛРП.
Необходимо обратить внимание на отсутствие достоверных отличий между периодами КО по таким периоперационным параметрам, как частота конверсий, продолжительность стационарного лечения и частота осложнений, что свидетельствует о повышении уровня мануальных навыков с накоплением опыта. Этому не противоречат достоверные отличия между периодами КО в объеме интраоперационной кровопотери (ЛРП), как правило увеличивающейся при повышении уровня сложности резекции, и времени операции (ЛРП и РАРП), что также закономерно. С накоплением опыта (завершение 2-го периода и 3-й период обучения) величина интраоперационной кровопотери и время операции уменьшились, несмотря на большую сложность РП в эти периоды обучения. При обучении ЛРП отмечены отличия в частоте конверсий между периодами. Увеличение частоты конверсии можно объяснить достоверно большим числом пациентов, перенесших операции на брюшной полости в группе ЛРП (спаечный процесс), а также фактом их преимущественного лечения во 2-м и 3-м периодах обучения.
Заключение
Метод кумулятивных сумм является универсальным способом оценки кривой обучения, применимым для изучения динамики различных периоперационных исходов РП. Основным показателем, позволяющим наиболее точно отразить освоение РП, следует считать сложность резекции, оцениваемую по специальным расчетным шкалам.
Прохождение КО РАРП оказывает существенное влияние на продолжительность и результаты КО ЛРП. Изменяется не только продолжительность периодов КО ЛРП, но и характер нозологий (увеличение числа пациентов со злокачественными опухолями печени, в том числе на ранних этапах КО). Предварительный опыт робот-ассистированных вмешательств позволил увеличить частоту лапароскопических резекций в условиях спаечного процесса после ранее перенесенных хирургических вмешательств на брюшной полости.
Участие авторов
Коваленко Д.Е. – сбор и обработка материала, статистическая обработка данных, написание текста.
Ефанов М.Г. – концепция и дизайн исследования, редактирование, утверждение окончательного варианта статьи, ответственность за целостность всех частей статьи.