Робот-ассистированный забор DIEAP лоскута: обзор методик
Аннотация
Роботизированная хирургия расширила возможности хирургической техники для человека, способствуя устранению тремора, эргономичному позиционированию, 3D-обзору и улучшенному разрешению изображения оперируемого поля.
Цель исследования: изучение техник забора DIEAP лоскута с применением миниинвазивных роботассистированных методик.
Материал и методы. Для обзора использовались базы данных PubMed, SCOPUS, ScienceDirect, Российской научной электронной библиотеки. Поиск проводили по ключевым фразам: «robotic deep inferior epigastric artery perforator flap», «robotic DEIAP», «роботическая хирургия молочной железы», «робот-ассистированная реконструкция молочной железы». Критериями включения в исследование являлись доклады о случаях применения методики или исследования на кадаврах.
Результаты. Были обнаружены девять исследований, соответствующих критериям включения, в которых рассматривался забор DIEAP лоскутов с применением робот-ассистированных технологий. Суммарное количество участников в этих исследованиях составило 59 человек. В пяти исследованиях авторы определяли технику забора лоскута как трансперитонеальную или интраперитонеальную. В одном исследовании был описан экстраперитонеальный забор лоскута. В трех исследованиях использовали одинаковую терминологию: трансабдоминальный преперитониальный и тотально экстраперитонеальный забор лоскута.
Заключение. Робот-ассистированный забор DIEAP лоскута может проводиться с использованием трансабдоминально преперитонеальной техники и тотально экстраперитонеально, а также с использованием монопортового и мультипортового доступов c различным расположением портов. Однако для более детального изучения рассматриваемого вопроса необходимо проведение рандомизированных исследований с контролем слабости передней брюшной стенки и сравнением осложнений в результате применения различных методов.
Ключевые слова: робот-ассистированная хирургия, роботическая хирургия, DIEAP, забор лоскута.
Конфликт интересов: авторы подтверждают отсутствие явного и потенциального конфликта интересов, о котором необходимо сообщить.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Для цитирования: Старцева О.И., Решетов И.В., Ермощенкова М.В., Габриянчик М.А., Абазалиева А.Д. Робот-ассистированный забор DIEAP лоскута: обзор методик. Вопросы реконструктивной и пластической хирургии. 2023. Т. 26, № 2. С. 13–24. doi 10.52581/1814-1471/85/02
Введение
Реконструкция молочной железы позволяет достичь восстановления и повысить качество жизни онкологических пациентов, перенесших мастэктомию. Золотым стандартом реконструкции являются применение аутологичных тканей (лоскуты передней брюшной стенки и широчайшей мышцы спины) и реконструкция с имплантами. Анализ применения перфорантного лоскута нижней эпигастральной артерии (the deep inferior epigastric artery perforator (DIEAP)) в исследованиях показал меньшую травматизацию мышц живота и значительное снижение риска развития слабости передней брюшной стенки, чем в случаях применения поперечного кожно-мышечного лоскута передней брюшной стенки на основе прямой мышцы живота [1–3].
Лоскут DIEAP является наиболее надежным для микрососудистой реконструкции молочной железы, демонстрируя благоприятные результаты и обеспечивая хороший долгосрочный эстетический результат. Тем не менее, остается значительный процент пациенток с жалобами на слабость передней стенки живота, что, возможно, связано с деруфикацией мышц и повреждением нервов, иннервирующих прямые мышцы живота, так как нижняя эпигастральная артерия проходит под прямой мышцей живота и чаще всего под нервами.
Травматизация нерва во время расслоения мышцы или его пересечение может привести к денервационной потере функции прямой мышцы живота на 30% через 1 год после операции [4]. К тому же во время забора DIEAP лоскута для достижения необходимой длины сосудистой ножки прибегают к значительному рассечению передней пластинки влагалища прямых мышц живота. Фасция обычно рассекается от выбранного перфоранта до паховой области ниже дугообразной линии (иногда длина разреза достигает 15 см). Для уменьшения факторов травматизации возможно применение миниинвазивных техник эндоскопии и роботассистированной хирургии, что позволяет достичь выделения сосудистой ножки через короткие разрезы. Более того, новые модели хирургических роботов позволяют проводить операцию через единичный порт.
Впервые роботизированная хирургия была применена в 1985 г. для деликатной и точной стереотаксической нейрохирургической биопсии [5–8]. Данный опыт побудил хирургов использовать робот для трансуретральной резекции предстательной железы. Последовало еще несколько итераций роботизированных платформ, включая робота-ассистента хирурга для простатэктомии. Эти роботизированные системы работали с использованием фиксированных анатомических ориентиров и поэтому не были адаптированы к операциям в пластической хирургии [5].
Для обеспечения более динамической хирургии были разработаны несколько различных роботизированных систем, но в конечном счете система Da Vinci (Intuitive Surgical Inc.) стала превалирующей в роботизированной хирургии. Технология улучшенной визуализации стала важным шагом в новой платформе, обеспечивая стабильное 3D-HD изображение операционного поля, одновременно предоставляя хирургу автономный контроль над 8-миллиметровым эндоскопом. По сравнению с громоздкими камерами предыдущих систем, 8-миллиметровая камера новой конструкции обеспечивает хирургу более четкий обзор операционного поля благодаря более яркому изображению.
Роботизированная хирургия расширила возможности хирургической техники, предложив устранение тремора, эргономичное позиционирование, 3D-обзор и улучшенное разрешение операционного поля. Одним из важных направлений в лечении на ранних стадиях рака молочной железы становится использование принципов органосохраняющих операций с элементами пластической хирургии и миниинвазивной эндовидеохирургии. Робот-ассистированная радикальная подкожная мастэктомия ассоциирована с низкой частотой возникновения ранних и поздних осложнений [9–12], а лимфоаксиллярная диссекция с применением методов роботической хирургии снижает вероятность возникновения послеоперационных осложнений и лимфедематозных ятрогенных осложнений [13]. Манипуляторы роботической системы позволяют оперировать в ограниченных операционном поле и полостях, поэтому их применение может сделать сложную микрохирургию более удобной [14, 15]. В хирургии молочной железы роботассистированная микрохирургия также применялась в реиннервации сохраненной кожи и сосково-ареолярного комплекса.
Цель исследования: изучение миниинвазивных робот-ассистированных техник забора DIEAP лоскута, как этапов в роботической хирургии молочной железы.
Материал и методы
Был проведен систематический обзор согласно протоколу PRISMA. В электронных базах данных за период с 2010 по 2022 г. был осуществлен поиск статей, в которых оценивались техники реконструкции молочных желез с применением миниинвазивных робот-ассистированных технологий для забора лоскутов передней брюшной стенки. Для обзора использовались базы данных PubMed, SCOPUS, ScienceDirect, Российской научной электронной библиотеки. Поиск проводили по ключевым фразам «robotic deep inferior epigastric artery perforator flap», «robotic DEIAP», «роботическая хирургия молочной железы», «робот-ассистированная реконструкция молочной железы».
Критерии включения в обзор: доклады о случаях применения рассматриваемой методики или исследования на кадаврах Данные были извлечены из статей и экстраполированы в таблицу.
Результаты
Было обнаружено девять исследований (суммарно 59 пациентов), соответствующих критериям включения данного обзора, в которых рассматривался забор DIEAP лоскутов с применением робот-ассистированных технологий. Из них у 5 пациентов (5 лоскутов) была выполнена одномоментная реконструкция [16–19], причем один случай описывает одномоментную реконструкцию после робот-ассистированной мастэктомии. Одно исследование включало 9 кадавров [17].
Описание методик, которые применялись в исследуемых статьях
| № | Название статьи | Локусы и количество пациентов | Техника забора лоскута | Время инсталляции робота | Время операции | Инсталляция портов | Интраоперационные осложнения | Инсуфляция |
|---|---|---|---|---|---|---|---|---|
| 1 | Implementing the Robotic deep inferior epigastric perforator Flap in daily practice: A series of 10 cases | 10 билатеральных DIEAP лоскутов. 9 пациентов с отсрочной реконструкцией, 1 пациенту выполнена одномоментная реконструкция | Трансперитонеальный мультипортовый робот-ассистированный забор лоскута | 16–40 мин | Робот-ассистированное время — 86 мин. Среднее операционное время — 479 мин | Три троакара введены контралатерально выбранному перфоранту по передней подмышечной линии через дефект после рассечения кожи для выделения лоскута, без дополнительных разрезов. Камера инсталлирована между двумя крайними портами | Нет | Пневмоперитоней 15 мм рт. ст. |
| 2 | Initial report of extraperitoneal pedicle dissection in deep inferior epigastric perforator flap breast reconstruction using the da Vinci SP | 1 билатеральный DIEAP лоскут. Пациент с одномоментной реконструкцией | Экстраперитонеальный монопортовый робот-ассистированный забор лоскута | Не указано | Не указано | Один порт инсталлирован через разрез кожи для непосредственного медиального края интраператной прямой мышцы живота | Нет | 12 мм рт. ст. |
| 3 | Robotic deep inferior epigastric perforator flap harvest in breast reconstruction | 4 пациента, 7 лоскутов (6 унилатеральных лоскутов с отсроченной реконструкцией, 1 билатеральный лоскут). Три лоскута забраны во время одномоментной реконструкции | Трансперитонеальный мультипортовый забор лоскута (TAPP) | Не указано | Не указано | Три троакара введены контралатерально выбранному перфоранту латерально первичной мышце живота через дефект после рассечения кожи для выделения лоскута, без дополнительных разрезов. Камера инсталлирована между двумя крайними портами | Нет | 10 мм рт. ст. |
| 4 | Robotic DIEP Flap Harvest through a Totally Extraperitoneal Approach Using a Single-Port Robotic System | 1 пациент без уточнений | Тотально экстраперитонеальный (TAPP) монопортовый забор лоскута | Не указано | Робот-ассистированное время (55 ± 33) мин. Среднее операционное время (487 ± 93) мин | Один порт инсталлирован через разрез кожи для медиального края интраперитональной прямой мышцы живота | Нет | 8 мм рт. ст. |
| 5 | Robotic-assisted deep inferior epigastric artery perforator flap abdominal harvest for breast reconstruction: A case report | 1 пациент, отсрочная реконструкция | Трансперитонеальный мультипортовый робот-ассистированный забор лоскута | Не указано | Не указано | Три троакара введены контралатерально выбранному перфоранту по передней подмышечной линии через дефект после рассечения кожи для выделения лоскута, без дополнительных разрезов на коже. Камера инсталлирована между двумя крайними портами | Нет | Пневмоперитоней 15 мм рт. ст. |
| 6 | Robotic versus Standard Harvest of Deep Inferior Epigastric Artery Perforator Flaps: Early Outcomes | 25 пациентов (15 с DIEP (30 лоскутов), 10 DIEP (20 лоскутов)). Применялась индоцианиновая зелень | Интраабдоминальный забор лоскута без уточнений | Не указано | Среднее робот-ассистированное время — 173 мин. Среднее операционное время — 759 мин | Не указано | Нет | Не указано |
| 7 | Robotic-Assisted DIEP Flap Harvest for Autologous Breast Reconstruction: A Comparative Feasibility Study on a Cadaveric Model | 8 кадаверов (16 hemi-DIEP лоскутов) | 16 hemi-DIEP лоскутов: 50% TAPP и 50% TEP | Не указано | Среднее время забора лоскута 56 мин (TAPP) 65 мин (TEP). Аутогрантации не проводилась | Порт камеры введен через надпупочный поперечный разрез (1.5–2 см). Второй 8-миллиметровый порт вводился интраабдоминально, третий 8-миллиметровый порт вводился через разрез кожи в линии разметки лоскута | В одном случае TAPP была травма кишки, и один случай TEP был переход на обычную открытую технику из-за пневмоторакса | 8 мм рт. ст. |
| 8 | The Robotic DIEP Flap | 1 пациент, отсрочная реконструкция | Трансперитонеальный мультипортовый робот-ассистированный забор лоскута | Не указано | Не указано | Три троакара введены контралатерально выбранному перфоранту по передней подмышечной линии через дефект после рассечения кожи для выделения лоскута, без дополнительных разрезов на коже. Камера инсталлирована между двумя крайними портами | Нет | Пневмоперитоней 15 мм рт. ст. |
| 9 | Robotic-assisted deep inferior epigastric perforator (DIEP) flap harvest for breast reconstruction | 1 пациент, одномоментная билатеральная реконструкция | Трансперитонеальный мультипортовый робот-ассистированный забор лоскута (intra-peritoneal approach) | Не указано | Среднее операционное время составило 10 часов (9 часов для заготовки, 1 час для диссекции лоскутов). 16 мин инсталляции | 10-миллиметровый порт для камеры был введен в надпупочной области, а 8-миллиметровые манипуляторные порты вводились через два разреза, расположенные на левой и правой наружной косой мышце | Нет | Не указано |
В пяти исследованиях техника забора лоскута была определена как трансперитонеальная или интраперитонеальная, что означает введение троакаров через париетальную брюшину и диссекцию нижней эпигастральной артерии из брюшной полости. В одном исследовании был описан забор лоскута, который определялся как экстраперитонеальный, что означало диссекцию без рассечения париетальной брюшины.
Из сказанного выше можно сделать вывод о том, что не существует устоявшегося конвенционального термина, описывающего техники робот-ассистированного забора лоскутов передней брюшной стенки. Только в трех исследованиях применялась одинаковая терминология: трансабдоминальный преперитониальный (что означало диссекцию сосудистой ножки из брюшной полости с рассечением париетальной брюшины) и тотально экстраперитонеальный (что означало диссекцию сосудистой ножки из препариетального пространства, т.е. без рассечения париетальной брюшины) [18–20].
Таким образом, для установления терминологии, которая согласуется с иностранными коллегами, трансперитонеальную и интраперитонеальную техники можно объединить в термин «Трансабдоминальный преперитонеальный (ТАПП) забор лоскута». «Тотально экстраперитонеальный (ТЭП) забор лоскута» (рис. 1) означает любую диссекцию из преперитонеального пространства.
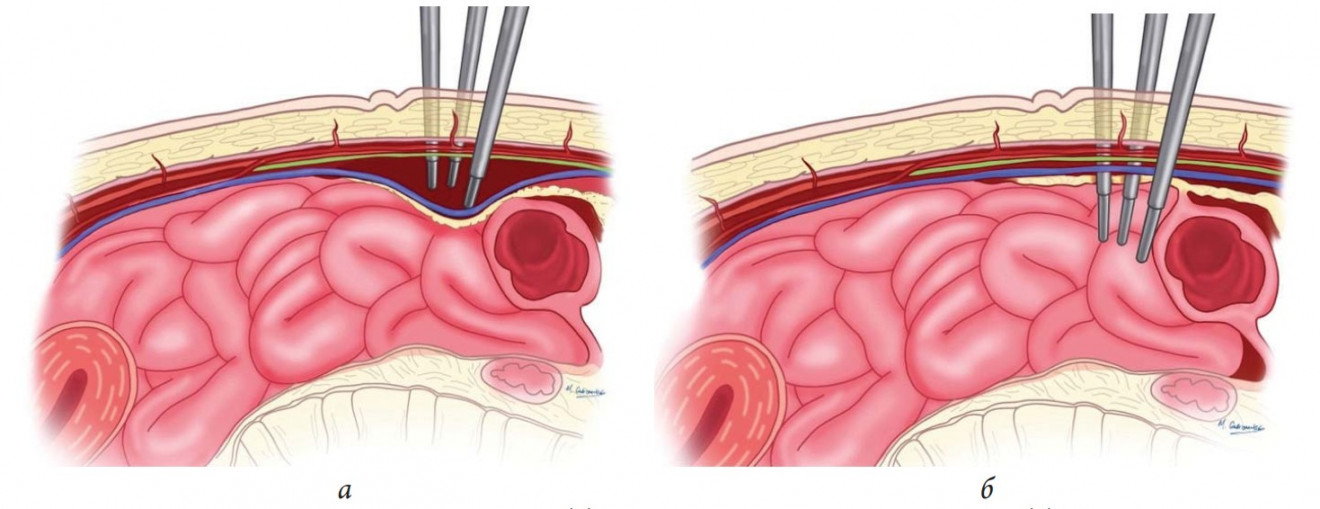 Рис. 1. Трансабдоминально преперитонеальный (а) и тотально
экстраперитонеальный (б) доступы для забора DEIAP лоскута (автор рисунка М.А. Габриянчик)
Рис. 1. Трансабдоминально преперитонеальный (а) и тотально
экстраперитонеальный (б) доступы для забора DEIAP лоскута (автор рисунка М.А. Габриянчик)
В настоящее время используются техники с применением нескольких портов (мультипортовые) и более современные – с одним портом (однопортовые). Поэтому в комбинации ТАПП и ТЭП с количеством используемых портов можно выделить четыре техники.
Трансабдоминальный преперитонеальный забор лоскута DIEAP
Техника ТАПП выполнялась с проникновением во внутрибрюшное пространство через разрез париетальной брюшины для вскрытия задней пластинки влагалища прямой мышцы живота и выделения глубокой нижней эпигастральной артерии. Операция при роботизированном ТАПП DIEP начиналась как при стандартном способе. Предварительно выбранный перфорант обнажали до поверхности прямой мышцы живота, производили небольшой (до 3 см) фасциальный разрез для проведения выделенной сосудистой ножки. Через трансабдоминальный порт создавали пневмоперитонеум с давлением от 10 до 15 мм рт. ст. Хирург за пультом определял направление нижних эпигастральных сосудов вдоль поверхности прямой мышцы, прямо под прозрачной оболочкой брюшины. Брюшину вскрывали, ножку отсекали и диссецировали до фасциального дефекта, созданного во время выделения перфоранта. При приближении диссекции к перфоранту возможна утечка газов из брюшной полости через фасциальный разрез, что можно контролировать с помощью лапаротомной прокладки.
Следующим этапом является извлечение всей сосудистой ножки через фасциальный разрез возле перфорната, что возможно выполнять двумя методами. Первый метод заключался в интраабдоминальном ушивании задней пластинки и брюшины с последующим извлечением сосудистой ножки. Для облегчения ушивания возможно снижение давления до 10 мм рт. ст. Второй метод отличался тем, что пневмоперитонеум временно устраняли, и фасциальный дефект возле перфоранта герметично ушивали.
Затем пневмоперитонеум воссоздавали, и выполняли ушивание задней пластинки и брюшины, после чего порты удаляли, и места портов послойно ушивали.
Тотально экстраперитонеальный забор лоскута DIEAP
Для доступа в предперитонеальное пространство и подготовки робота сначала выполняется фасциальный разрез длиной 1,5 см вдоль полулунной линии на ипсилатеральной для сосудистой ножки стороне. Через этот разрез выполняется преперитонеальная тупая диссекция указательным пальцем для получения объема рабочего пространства. Осуществляют осторожное тупое расслоение предбрюшинного пространства с помощью видеокамеры робота, чтобы уменьшить вероятность разрывов брюшины. Во время этого маневра в преперитонеальное пространство нагнетается углекислый газ под давлением от 8 до 12 мм рт. ст. Из-за отсутствия задней пластинки влагалища прямой мышцы ниже дугообразной линии эта область более подвержена расширению.
Ось рычагов инструмента направлена к наружной подвздошной артерии. Камера установлена на нижней стороне привода, а другие роботизированные рычаги закреплены на боковой и верхней сторонах, что предотвращает попадание роботизированных рычагов в дугообразную линию. Затем выявляют глубокие нижние эпигастральные сосуды, отсекают и диссецируют до одного или нескольких перфорантов, все сосудистые ветви перевязывают.
Возможные расположения портов
При ТАПП и ТЭП доступах порты устанавливаются, как через предполагаемые разрезы кожи, т.е. по линиям разметки DIEAP лоскута и неопупка, так и через разрезы, которые уже были выполнены в ходе операции (рис. 2).
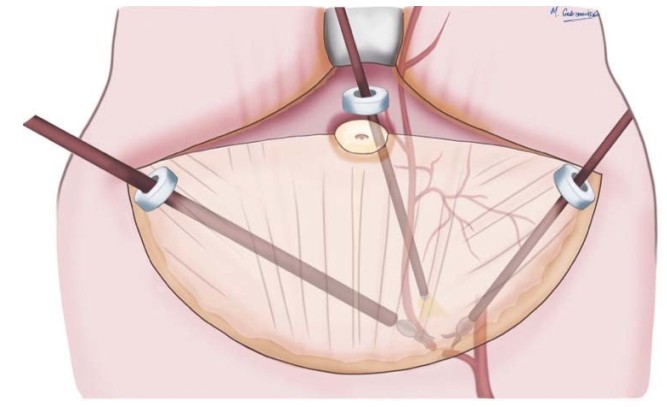 Рис. 2. Пример установки троакаров через уже выполненные
разрезы кожи и подкожно-жировой клетчатки (автор рисунка М.А. Габриянчик)
Рис. 2. Пример установки троакаров через уже выполненные
разрезы кожи и подкожно-жировой клетчатки (автор рисунка М.А. Габриянчик)
Первый способ позволяет сохранять кожные покровы интактными, что делает пневмоперитонеум и пневмопредперитонеум более герметичными. При втором методе в начале операции стандартно выделяют лоскут, определяют надежные перфоранты, и только потом рассекают фасцию на 1–3 см, что облегчает хирургу навигацию.
Монопортовое расположение манипуляторов достигается установлением порта через неопупок. При мультипортовом расположении возможно вертикальное и горизонтальное расположение. Вертикальная установка допускается только при предварительном выделении кожно-жирового лоскута, когда три троакара вводят контрлатерально выбранному перфоранту по передней подмышечной линии после рассечения кожи для выделения лоскута, без дополнительных разрезов на коже. Порт для камеры устанавливают между двумя крайними портами по передней подмышечной линии. Во время горизонтальной мультипортальной установки порт камеры вводят через надпупочный поперечный разрез белой линии длиной 1,5–2,0 см. Второй 8-миллиметровый порт вводят ипсилатерально по дугообразной линии, третий 8-миллиметровый порт устанавливают контралатерально по дугообразной линии или латеральнее через наружную косую мышцу.
Обсуждение
Роботизированный забор лоскутов предположительно может уменьшить развитие отсроченных осложнений, связанных с денервацией прямых мышц живота, травматизацию.
Трансабдоминальный преперитонеальный способ забора DIEAP лоскута опасен возникновением специфических абдоминальных интра- и постоперационных осложнений, таких как абдоминальный компартмент-синдром, повреждение магистральных забрюшинных сосудов, органов желудочно-кишечного тракта, а также инфекционными осложнениями. Возможны ошибки наложения пневмоперитонеума, которые могут привести к развитию подкожной и предбрюшинной эмфиземы.
Тотальный экстраперитонеальный способ позволяет избежать рассечения париетальной брюшины, что, возможно, значительно снижает риски развития специфических осложнений, однако необходимость увеличения объема предперитонеального пространства может повлиять на кислотно-щелочной баланс организма и интраабдоминальное давление, особенно у коморбидных пациентов. Для более детального изучения необходимо проведение рандомизированных исследований с контролем слабости передней брюшной стенки и со сравнением осложнений различных методов.
В клинической практике необходим контроль кровотечения и других грозных осложнений, вынуждающих хирургов перейти к открытому способу. Следует отметить, что ни в одном из рассматриваемых исследований авторами не было указано о таком развитии клинической ситуации. Роботически-ассистированный забор лоскутов в зависимости от законодательной практики страны и опыта хирургов может выполняться как командой пластических хирургов, так и междисциплинарной командой с привлечением абдоминальных хирургов.
Заключение
Популяризируя роботический забор DIEAP лоскута, хирурги делают вклад в развитие концепции миниинвазивной роботической реконструктивной хирургии молочной железы. Данная концепция включает роботически-асситированные операции и этапы: мастэкомию с сохранением кожи и сосково-ареолярного комплекса, роботическую реиннервацию сохраненной кожи и сосково-ареолярного комплекса, роботические забор DIEAP лоскута и наложение микрохирургических анастомозов, наложение лимфо-венулярных анастомозов.








