Использование роботического комплекса Da Vinci в хирургии грыж. Опыт клиники
Введение
В последнее 10-летие набирает все большую популярность робототехника в различных направлениях хирургии, однако мы не встретили большого количества публикаций, посвященных данному направлению оперативного лечения грыж в отечественных изданиях.
Подробно в научной литературе описаны техники тотальных экстраперитонеальных и трансабдоминальных вмешательств с использованием лапароскопических инструментов. Несмотря на это, часть экспертов считает, что возможно улучшить результаты лечения пациентов, используя роботические технологии, а также отмечает преимущества в удобстве этих операции для хирурга.
Цель нашей работы — описание собственного опыта хирургии грыж с использованием роботизированного комплекса, а также анализа места данной методики в мире.
Материал и методы
В период с 2021 по 2023 г. в Ильинской больнице было выполнено 17 операций. Из них пациенты, оперированные по поводу вентральной грыжи, составили 7 случаев, паховой грыжи — 8 случаев, пупочной грыжи — 2 случая.
Приводим список часто используемых аббревиатур:
- IPOM — intraperitoneal onlay mesh — лапароскопическая операция с протезированием изнутри брюшной стенки сетчатым композитным имплантом;
- eTEP — Extended totally extraperitoneal repair — техника операции в расширенном экстраперитонеальном пространстве;
- eTEP-RS — Extended totally extraperitoneal repair Rives and Stoppa — техника операции в расширенном экстраперитонеальном пространстве с установкой сетчатого импланта ретромускулярно (позади прямых мышц живота), как это было предложено хирургами Rives и Stoppa; — eTEP-RS-TAR — Extended totally extraperitoneal repair Rives and Stoppa with transversus abdominis release — техника операции в расширенном экстраперитонеальном пространстве с этапом пересечения поперечной мышцы живота с одной или двух сторон и установкой сетчатого импланта ретромускулярно (позади прямых мышц живота), как это было предложено хирургами Rives и Stoppa;
- TAPP — Transabdominal pre-peritoneal — операция трансабдоминальным доступом с рассечением брюшины и установкой сетчатого импланта под нее;
- vTAPP — ventral Transabdominal pre-peritoneal — операция трансабдоминальным доступом с рассечением брюшины и установкой сетчатого импланта под нее, используемая при лечении вентральных и пупочных грыж;
- TARUP — Transabdominal retromuscular umbilical prosthetic hernia repair — трансабдоминальныя ретромускулярная пластика пупочной грыжи, сопровождающаяся рассечением заднего листка влагалища прямой мышцы
При наличии вентральной грыжи выполнены следующие операции: IPOM+ — в 3 случаях, 2 операции выполнены по методике eTEP-RS и в 2 случаях — eTEP-RS-TAR. При паховых грыжах пациенту выполняли трансабдоминальную преперитонеальную герниопластику TAPP. При пупочных грыжах выполнили в 1 случае TARUP и в 1 случае vTAPP. Из 17 пациентов 13 были мужчины, а 4 — женщины. Средний возраст больных 60 лет. Средний индекс массы тела — 28 кг/м2. Большинство больных имели хороший физический ASA 1 — 1, ASA 2 — 14, у 2 пациентов — ASA 3. Данные пациентов представлены в табл. 1. Все оперативные вмешательства выполнялись под общей анестезией.
| Данные пациентов Me, Q [25%; 75%] | Сопутствующие заболевания
|
n/%
|
|
| Число пациентов
|
17
|
Гипертоническая болезнь
|
5/29,4
|
| Пол (М/Ж) | 76,5/23,5
|
Гиперлипидемия | 4/23,5
|
| Возраст, лет
|
60 [52; 73] | ГЭРБ | 1/5,9
|
| ИМТ, кг/м2
|
28 [26; 29,4]
|
Сахарный диабет | 3/17,6 |
| Шкала ASA, баллы
|
2 [2; 3] | Бронхиальная астма
|
4/23,5
|
| ТЭЛА
|
0/0 | ||
| ХОБЛ
|
1/5,9
|
||
| Рак яичников
|
1/5,9 | ||
| Типы оперативных вмешательств
|
n/% | ||
| Вентральные грыжи | |||
| IPOM+
|
3/17,6
|
||
| eTEP
|
2/11,8
|
||
| eTEP+TAR
|
2/11,8
|
||
| Паховые грыжи | |||
| TAPP
|
8/47,1
|
||
| Пупочные грыжи
|
|||
| TARUP | 1/5,9
|
||
| vTAPP
|
1/5,9
|
||
Таблица 1. Демографические и периоперационные данные пациентов
Паховые грыжи. Техника выполнения операций
При выполнении операций по поводу паховых грыж мы делали разрез кожи над пупком и формировали карбоксиперитонеум 12 мм рт.ст. при помощи иглы Вереша, далее через этот разрез устанавливали первый 12 мм троакар для оптической системы. При этом необходимо учитывать толщину передней брюшной стенки пациента, потому что в случае небольшой оставшейся свободной части троакара над кожей могут возникнуть трудности с фиксацией к нему оптической руки-манипулятора. Дополнительные 8 мм троакары устанавливались справа и слева в мезогастральной области (рис. 1). Для визуализации мы использовали стандартную 30° роботическую оптическую систему Intuitive. Операцию выполняли в стандартном объеме согласно «critical view of myopectineal orifice» (рис. 2). Во всех случаях использовался облегченный полипропиленовый имплантат размерами 10×15 см, который фиксировали одиночными швами в 3—4 точках или не фиксировался вовсе. Брюшину ушивали рассасывающейся нитью V-loc 180 3-0.
Вентральные грыжи. Техника выполнения операций
Операции по поводу вентральных грыж выполняли по технике IPOM, eTEP или eTEP (TAR) с унилатеральным пересечением поперечных мышц живота. Ход операции доступом eTEP был идентичным технике, описанной И. Белянским в статье «Early operative outcomes of endoscopic (eTEP access) robotic-assisted retromuscular abdominal wall hernia repair». Положение на операционном столе: пациент лежит на спине с приведенными к телу руками в положении «перочинного ножа» с разгибанием тела в области поясницы. Операционное поле обрабатывается от лонного сочленения до реберных дуг. Разрез 10 мм для оптической системы выполняли в мезогастрии над прямой мышцей живота, затем при помощи оптического троакара visiport проникали в ретромускулярное пространство, производя тупую диссекцию в краниальном или каудальном направлении, далее, в зависимости от локализации грыжи, выполняли верхний или нижний кроссовер (переход в ретромускулярное пространство с противоположной стороны). При локализации срединной грыжи в верхней части живота мы выполняли нижний кроссовер (рис. 3), при локализации грыжи в нижней части выполняли верхний кроссовер (рис. 4). Мы не будем заострять внимание на технике операции, она детально описана в статье И. Белянского.
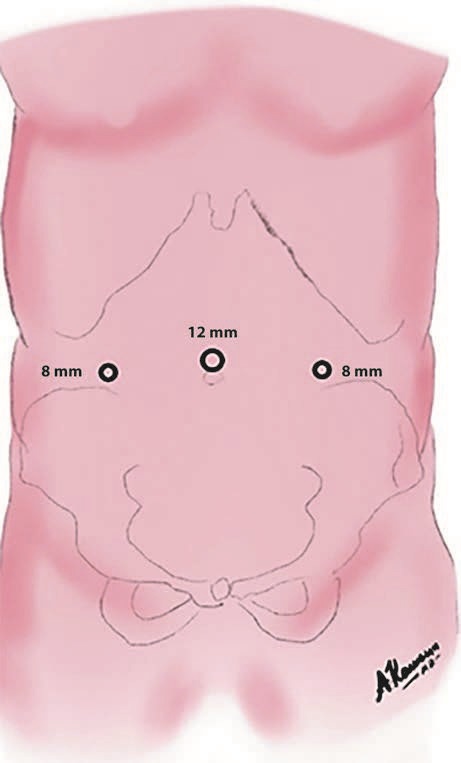
Рис. 1. Расположение троакаров.
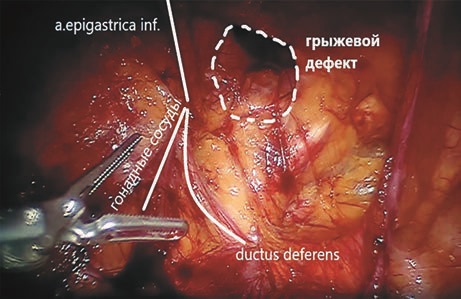
Рис. 2. Анатомия паховой области. Интраоперационная фотография.
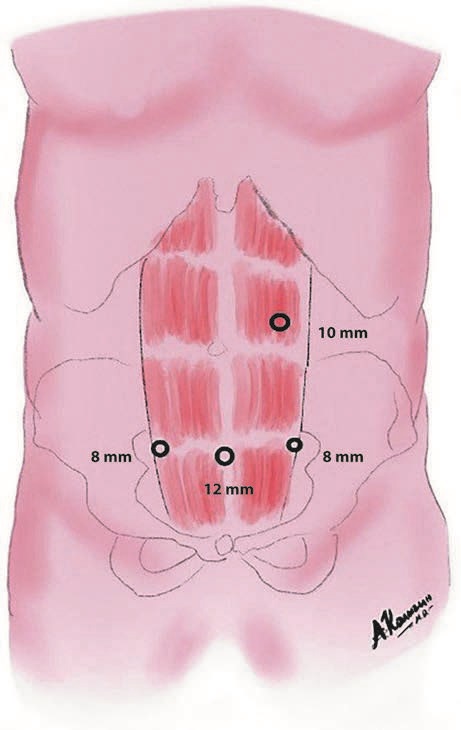
Рис. 3. Расположение троакаров.
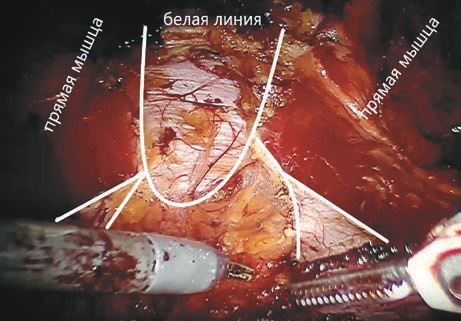 Рис. 4. Ретромускулярное пространство области. Интраоперационная фотография.
Рис. 4. Ретромускулярное пространство области. Интраоперационная фотография.
Операции по методике IPOM выполняли в положении пациента на спине, при этом руки пациента должны быть разведены в стороны, что дает больше места для работы роботических манипуляторов. Желательно, чтобы тело пациента было смещено на край стола, находящийся ближе к роботическому комплексу. Например, если вы имеете дело с боковой грыжей в правой половине живота, то лучше сдвинуть тело больного больше к левому краю. Такая позиция тела пациента даст больше свободы для движения манипуляторов. Разгибать тело пациента при данной операции, как правило, нет необходимости. Операционное поле обрабатывается и укрывается максимально латерально. Далее мы создавали карбоксипериотнеум 12 мм рт.ст., как правило, используя иглу Вереша в точке Палмера. Порты устанавливали в левой боковой области живота по принципу триангуляции. После низведения содержимого грыжевого мешка грыжевые ворота ушивали нерассасывающейся нитью V-loc PBT, и затем переднюю брюшную стенку протезировали композитным сетчатым имплантатом, фиксируя его к брюшной стенке по принципу «double-crown fixation».
Пупочные грыжи. Техника выполнения операций
При наличии пупочных грыж операции выполняли трансабдоминальным доступом с установкой сетчатого импланта в предбрюшинное пространство (vTAPP), либо в ретромускулярное пространство через разрез заднего листка влагалища прямых мышц живота (TARUP).
При выполнении данной операции пациент находился на операционном столе в положении лежа на спине. Технические приемы выполнения данной операции схожи с таковыми при IPOM, т.е. лучше чтобы больной лежал ближе к краю стола со стороны оператора с отведенной в сторону верхней конечностью. Порты обычно устанавливали в левой половине живота, предварительно сформировав карбоксиперитонеум до 12 мм рт.ст. в точке Палмера (рис. 5).
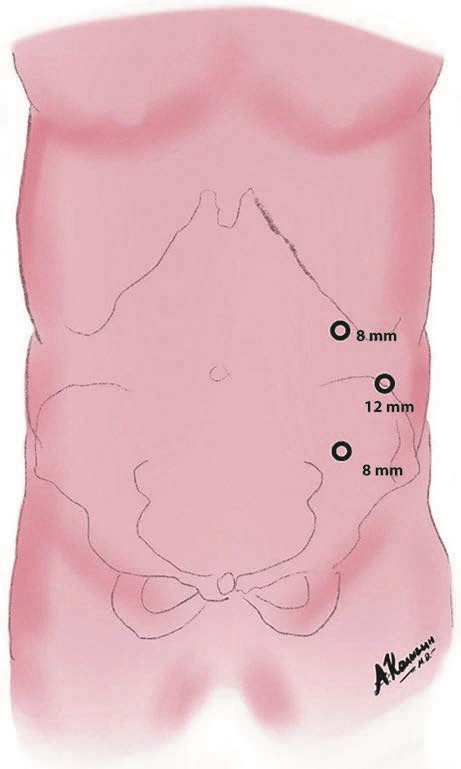
Рис. 5. Расположение троакаров при IPOM.
Брюшину от передней брюшной стенки аккуратно отсепаровывали на достаточном расстоянии от грыжевого дефекта, стараясь избегать травмы брюшины. Грыжевой дефект ушивали непрерывно нерассасывающейся нитью V-loc PBT укладывается имплантат на переднюю брюшную стенку, который может быть фиксирован несколькими одиночными узлами рассасывающейся нити. Брюшину ушивали непрерывно рассасывающейся нитью V-loc. Операция с установкой сетчатого имплантата в ретромускулярное пространство отличается лишь этапом вскрытия заднего листка влагалища прямой мышцы живота. При этом необходимо помнить, что слишком латеральное вскрытие заднего листка может привести к травме сосудисто-нервных пучков ретромускулярного пространства.
Результаты
Среднее время операции составило 2 ч 38 мин, минимальное время операции было 1 ч 35 мин, максимальное — 10 ч 11 мин. Интраоперационное осложнение было в одном случае — кровотечение из надчревной артерии. Сроки наблюдения пациентов составили от 3 мес до 3 лет. Ни в одном случае не выявлено рецидива грыж. Послеоперационные осложнения отмечены в 2 случаях, у одного пациента диагностирован эпидидимит после TAPP и у 1 пациента отмечена серома после eTEP-RS, все осложнения купированы консервативными мероприятиями. Интраоперационные осложнения были в 1 случае — кровотечение из a. epigastrica inferior, диагностированное после удаления троакара в конце операции и остановленное прошиванием кровоточащего сосуда. Статистические периоперационные данные представлены в табл. 2.
| Всего
|
TAPP
|
IPOM+
|
TARUP
|
eTEP
|
eTEP+TAR
|
|
| Длительность, мин
|
218 [170; 347]
|
184 [160,25; 206]
|
170 [158; 266]
|
219 | 308
|
550,5 [520,25; 580,75]
|
| Размер грыжи (наибольшее измерение), см
|
3 [3; 6]
|
3 |
6 [5,5; 7]
|
3 |
4 [3; 5]
|
10 [8,5; 11,5]
|
| Размер сетки (наибольшее измерение), см
|
15 [15; 15] | 15 |
15 [13,5; 15]
|
10
|
27,5 [26,25; 28,75]
|
26 [25,5; 26,5]
|
| Площадь сетки, см2
|
150 [150; 225]
|
150 | 225 [184,5; 225]
|
100
|
412,5 [393,75; 431,25] | 452,5 [428,75; 476,25]
|
| Госпитализация, сут | ||||||
| Интраоперационные осложнения, n (%)
|
1 (6,25) кровотечение | 0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
1 (50) кровотечение |
| Clavien—Dindo
|
||||||
| I, n (%)
|
2 (12,5) | 1 (11,1) | 0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
1 (50)
|
| II, n (%)
|
0 (0,0) | 0 (0,0)
|
0 (0,0) | 0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
| IIIa, n (%)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0) | 0 (0,0)
|
| IIIb, n (%)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0) | 0 (0,0)
|
0 (0,0) |
| IV, n (%)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0)
|
| V, n (%)
|
0 (0,0)
|
0 (0,0)
|
0 (0,0) | 0 (0,0)
|
0 (0,0) | 0 (0,0)
|
Таблица 2. Периоперационные данные
Обсуждение
Впервые в мире роботическую операцию по поводу грыжи выполнили в 2003 г. на животном [1]. А первую серию операций по поводу вентральных грыж доложили в 2012 г. [2]. Параллельно с роботической техникой развивалось лапароскопическое направление операций. В том же 2012 г. хирург Jorge Daes представил свою технику операции расширенной тотальной экстраперитонеальной пластики (eTEP), что позволило выполнять операции доступом в любой точке передней брюшной стенки [3]. Данная техника сделала возможным операции с установкой сетчатого импланта в ретромускулярное пространство (позади прямых мышц живота), предложенное еще в открытом доступе Rives и Stoppa. При сложных формах грыж или больших размерах грыжевых ворот, когда в ходе пластики имеется опасность большого натяжения на швах, на помощь может прийти прием пересечения поперечных мышц живота (eTEP TAR), описанные Belyansky и Novitsky [4, 5]. Однако развитию новых техник в герниологии мешали объективные трудности, такие как необходимость выполнения операции в условиях ограниченного пространства и формирования шва в непривычном положении («шов на потолке»). Например, I. Belyansky считает, что лапароскопический экстраперитонеальный доступ по-прежнему ограничивает доступные степени свободы и создает серьезные эргономические проблемы для оперирующего хирурга [6]. Часть экспертов полагает, что преодолеть эти трудности возможно используя роботизированные хирургические системы. Обладая стабильной камерой, возможностью широкого маневра манипуляторами, роботический комплекс способен сгладить трудности, возникающие в ходе операции.
Другая часть экспертов скептически относится к роботическим технологиям, отмечая сравнимые с лапароскопическими результаты операций, они указывают на большую стоимость роботических вмешательств. В своем исследовании F. Muysoms и M. Vierstraete сравнили роботические и лапароскопические паховые герниопластики. Исследователи не обнаружили разницы в количестве дней госпитального лечения и осложнений, однако средняя стоимость роботической операции составила €2612 против €1963 в группе лапароскопических операций [7, 8]. К аналогичным выводам приходят L. Solaini и D. Cavaliere, сравнивая лапароскопические и роботические паховые герниопластики в своем систематическом анализе [9]. Сторонники роботических операций все же отмечают положительные клинические аспекты данных вмешательств. Так, в метаанализе R. Dixit и соавт. провели систематическое обобщение имеющихся данных о влиянии лапароскопических и роботических вентральных герниопластик на результаты лечения, сообщенные пациентами, — Patient-Reported Outcome Measures (PROM). В анализ были включены 8 исследований с участием 41 205 участников. Возвращение к повседневной деятельности, возвращение к работе и частота рецидива были статистически лучше в группе роботических операций. Продолжительность госпитализации, повторная госпитализация, послеоперационная боль, качество жизни, внешний вид и удовлетворенность пациентов были одинаковыми в обеих группах [10]. Сторонники роботических операций отмечают более быстрое обучение этим операциям по сравнению с лапароскопическими.
Заключение
Таким образом, в настоящее время нет единого мнения о целесообразности выполнения роботических операций в герниологии. Преимущества минимально инвазивных методов герниопластики очевидны, а использование роботизированной платформы помогает увидеть эти преимущества. Исследования с более высоким уровнем доказательности могут прояснить более точные ранние и долгосрочные результаты, наши текущие данные поддерживают надежность и воспроизводимость роботизированной системы.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.










