Робот-ассистированные технологии (da Vinci) в гинекологической практике
В настоящее время эндовидеохирургия представляет одно из наиболее перспективных направлений в лечении различных гинекологических заболеваний. Ежегодно в клинике Национального медико-хирургического центра им. Н. И. Пирогова выполняется более 1000 подобных операций. Внедрение эндоскопических технологий в клиническую практику позволило коренным образом пересмотреть принципы хирургического лечения патологических состояний органов женской половой сферы. Технический прогресс не стоит на месте, появляются современные аппараты и инструменты для эндохирургических вмешательств, совершенствуются и разрабатываются новые методики эндоскопических операции 1.
Хирургический робот da Vinci стал самой крупной технологической разработкой последних десятилетий. В первый раз роботизированную систему в оперативной гинекологии использовали в 2005 г. в США. Многие хирурги-гинекологи предпочли эту технологию традиционной лапароскопии в связи с воплощением в ней ряда технологических инноваций. По инициативе Национального медико-хирургического центра им. Н. И. Пирогова в начале 2009 г. в России зарегистрировано использование новой медицинской технологии «робот-ассистированная эндовидеохирургия».
С 2009 г. в гинекологической практике с применением роботизированного комплекса da Vinci нами выполнены 273 операции. Среди них 207 радикальных и 66 органосохраняющих вмешательств: гистерэктомия произведена 114 пациенткам, пангистерэктомия в сочетании с тазовой лимфаденэктомией — 50, пангистерэктомия в сочетании с тазовой и парааортальной лимфаденэктомией — 2, миомэктомия — 41, иссечение эндометриоидного инфильтрата — 25, перитонеальный кольпопоэз — 8, сакрокольпопексия — 22, другие операции — 9. Еще двум больным выполнены симультанные операции по поводу патологии органов женской половой сферы в сочетании с раком толстой кишки.
Основными показаниями к операции служили миома матки, в том числе в сочетании с аденомиозом и гиперпластическими процессами эндометрия; атипическая гиперплазия эндометрия, рак тела и шейки матки, рак или пограничная опухоль яичников, распространенный ретроцервикальный эндометриоз с прорастанием соседних органов, выпадение купола влагалища после пангистерэктомии, врожденный порок развития — синдром Рокитанского — Кюстнера.
Не секрет, что кроме ряда технических преимуществ, улучшающих визуализацию и манипулирование, робот обладает некоторыми недостатками, среди которых наиболее существенными являются высокая стоимость, ограничение мобильности и отсутствие обратной тактильной связи. Наиболее эффективно, на наш взгляд, использование робота при работе в труднодоступных анатомических областях, при необходимости выполнения обширной диссекции, наложения большого количества швов. Учитывая преимущества и недостатки роботизированного комплекс da Vinci, целесообразно его внедрять в онкогинекологической практике, в хирургическом лечении тяжелых форм эндометриоза, пролапса тазовых органов.
В странах Западной Европы и Америки выполнение роботизированных операций по поводу онкозаболеваний является «золотым стандартом» 2. В течение последних 5 лет приблизительно 60% случаев рака эндометрия оперируются в США при помощи роботов, за относительно короткий срок они заменили лапароскопические и открытые операции 3. В нашей клинике выполнены 64 расширенные операции в сочетании и тазовой и парааортальной лимфаденэктомией, оментэктомией. В основном их производили пациенткам с раком эндометрия (n = 41), реже — с раком шейки матки (n = 16), с раком или пограничной опухолью яичников (n = 2), со сложной гиперплазией эндометрия с атипией (n = 5).
Во всех случаях обязательно проводилась идентификация тазового отдела мочеточника, его выделение до места пересечения с маточной артерией. Подвздошная лимфаденэктомия предполагает удаление трех групп лифоузлов. Цепочка узлов, лежащая латеральнее наружной подвздошной артерии, удалялась до уровня бифуркации общей подвздошной артерии. Диссекция узлов, расположенных по внутреннему краю наружной подвздошной вены, проводилась до стенки таза. Удаление лимфоузлов, лежащих по передней поверхности наружной подвздошной вены, производилось до уровня запирательного нерва. Удалялись также узлы, лежащие в области бифуркации подвздошных сосудов. Самым опасным этапом тазовой лимфаденэктомии является удаление клетчатки из запирательного пространства (рис. 1).
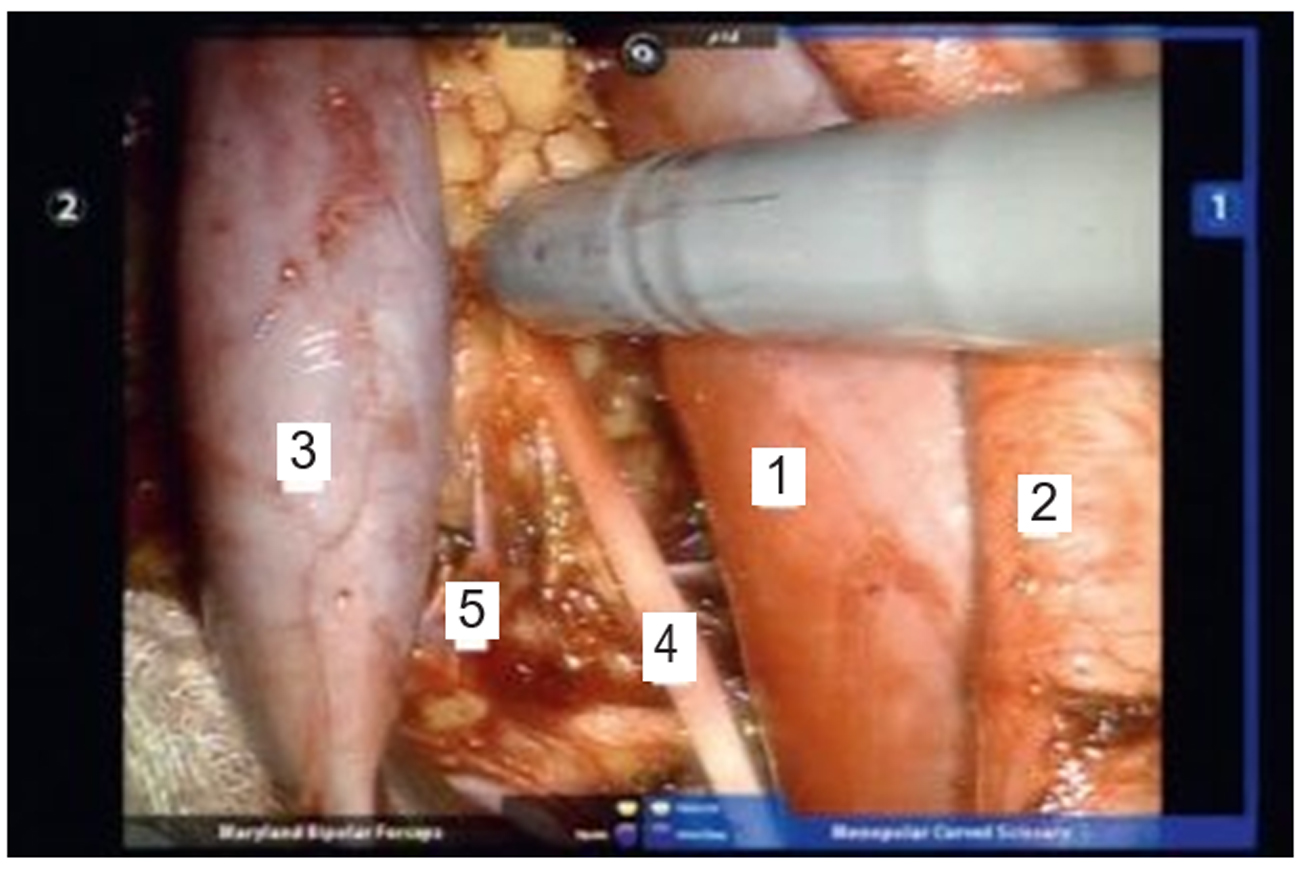 Рис. 1. Скелетирование запирательной ямки
с выделением запирательного нерва: 1 — поясничная мышца; 2 — наружная подвздошная артерия; 3 — наружная подвздошная вена; 4 — запирательный нерв; 5 — ветви внутренней подвздошной вены.
Здесь и далее в статье фото А. К. Политовой
Рис. 1. Скелетирование запирательной ямки
с выделением запирательного нерва: 1 — поясничная мышца; 2 — наружная подвздошная артерия; 3 — наружная подвздошная вена; 4 — запирательный нерв; 5 — ветви внутренней подвздошной вены.
Здесь и далее в статье фото А. К. ПолитовойМы использовали околопузырный доступ, который позволяет осуществлять четкий визуальный контроль на уровне дистальной трети запирательного пространства. Доступ обеспечивается между наружными подвздошными сосудами (латерально) и ветвями внутренних подвздошных сосудов (медиально) после удаления подвздошной клетчатки до уровня отхождения верхней пузырной артерии. При этом достигается адекватная визуализация дистальных ветвей внутренней подвздошной артерии, из которых и возникают чаще всего массивные кровотечения.
В 2 случаях выполнялась парааортальная лимфаденэктомия, отсепаровывались и удалялись клетчаточно-лимфатические пакеты, расположенные слева от аорты, спереди и сбоку от нижней половой вены и между ними до уровня нижней брыжеечной артерии (рис. 2).
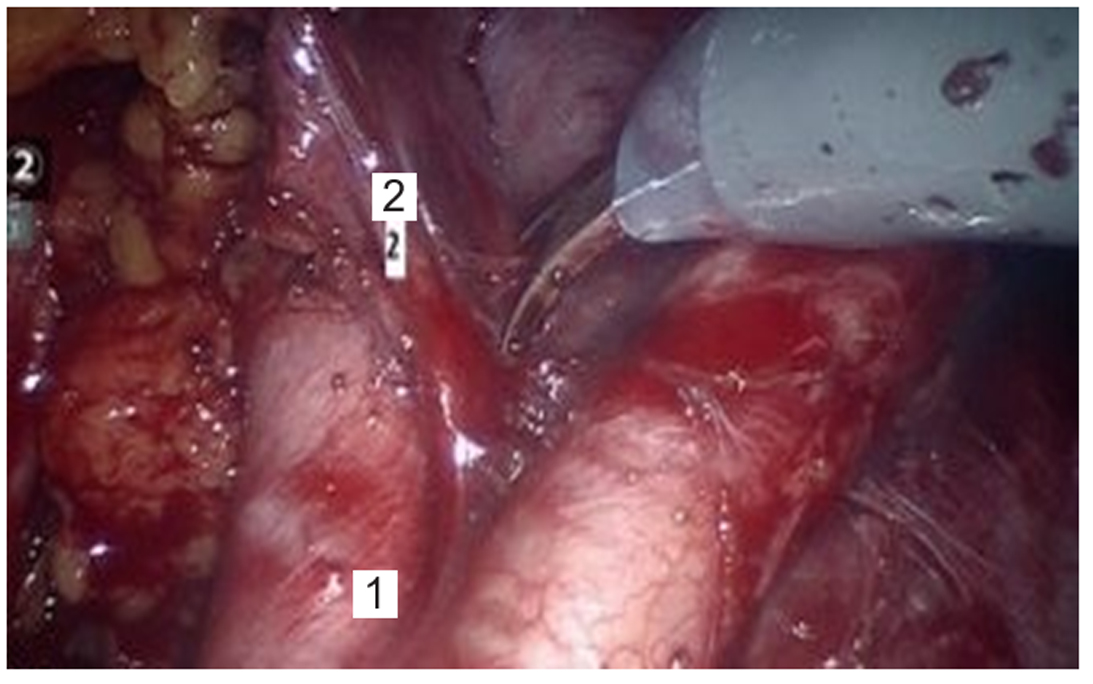 Рис. 2. Парааортальная лимаденэктомия:
1 — бифуркация аорты, 2 — клетчаточно- лимфатический пакет
Рис. 2. Парааортальная лимаденэктомия:
1 — бифуркация аорты, 2 — клетчаточно- лимфатический пакетРоботизированный комплекс позволяет выполнять флюоресцентную эндоскопию, что облегчает и повышает эффективность лимфаденэктомии за счет улучшения визуализации лимфоузлов.
Следует отметить, что робот дает возможность у данной категории пациенток осуществлять прецизионную лимфодиссекцию и адекватное хирургическое стадирование, нервосберегающие операции, удалить большее, чем при лапаротомии, количество лимфоузлов, а также снижает вероятность лимфореи и образования лимфокист в послеоперационном периоде.
Широкое внедрение роботизированных технологий в онкогинекологию, возможно, изменит всю философию подхода к лечению онкогинекологической патологии и значительно улучшит его результаты у этой достаточно сложной категории пациенток.
В клинике имееся небольшой опыт выполнения сакрокольпопексии — 22 операции. Показанием к операции являлось выпадение купола влагалища после гистерэктомии. Выделялись лобково-шеечная фасция, прямокишечно-влагалищная фасция с последующим фиксированием узловыми швами Y-образной полипропиленовой сетки Gynemech к стенкам влагалища и передней связке крестца. Данная сетка обладает превосходной прочностью и достаточной пористостью для прорастания ткани сквозь нее. Ее плетение обеспечивает эластичность в двух направлениях, что позволяет адаптироваться к различным изменениям, возникающим в организме.
Расширенный объем движений инструментов роботизированного комплекса облегчает интракорпоральное наложение швов. Инструменты, обеспечивая непревзойденную управляемость, дают возможность уверенно и ловко манипулировать тонкими тканями. Надежное обращение с тканями требует модуляции силы захвата ткани с помощью главных контроллеров. Облегчается наложение швов между имплантатом и анатомическими структурами. Фиксирование сетки к проманториуму — один из самых сложных этапов операции, сопряженный с риском развития кровотечения из крестцовых сосудов (рис. 3).
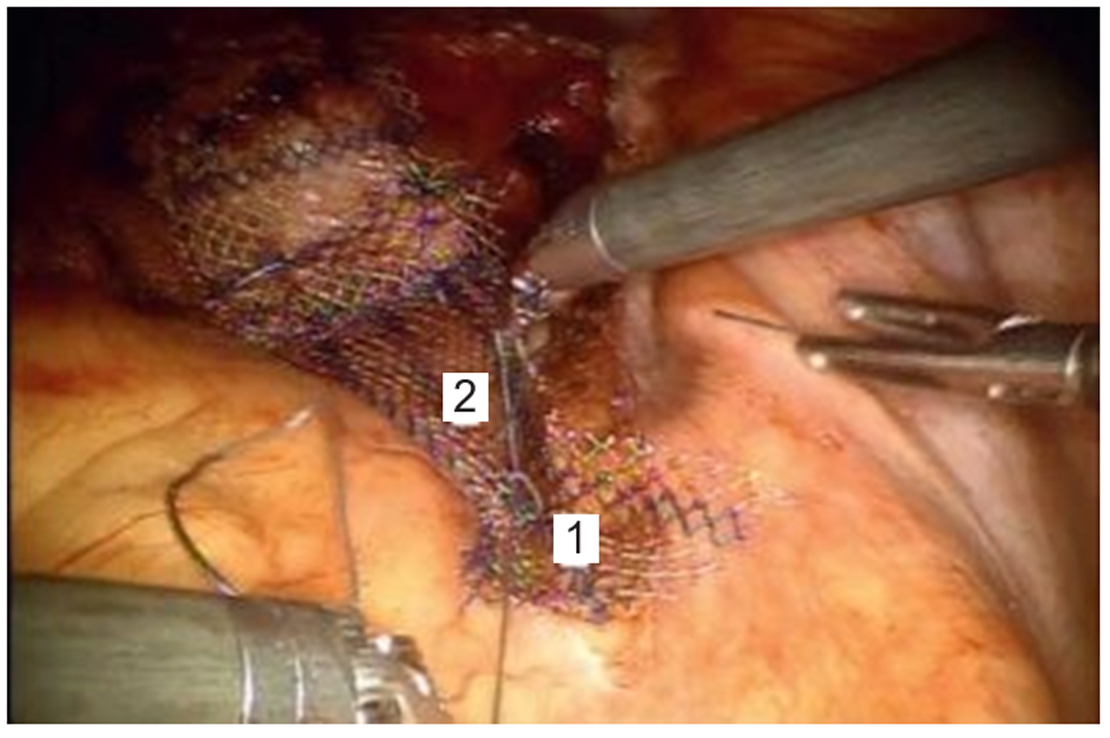 Рис. 3. Фиксация Y-образной сетки к передней связке крестца с помощью 2 узловых нерассасывающихся швов: 1 — проманториум; 2 — полипропиленовая сетка Gynemech
Рис. 3. Фиксация Y-образной сетки к передней связке крестца с помощью 2 узловых нерассасывающихся швов: 1 — проманториум; 2 — полипропиленовая сетка GynemechСакровагинопексия является операцией выбора при выраженном апикальном пролапсе гениталий, дает хорошие результаты, низкую частоту интра- и послеоперационных осложнений 4. Использование синтетических материалов у данной категории пациенток, учитывая роль дисплазии соединтельной ткани в патогенезе заболевания, необходимо, оно позволяет значительно уменьшить частоту рецидивов. Доля успешных результатов — 96%.
По поводу глубокого ретроцервикального эндометриоза в нашей клинике выполнены 25 робот-ассистированных операций. Иссечение эндометриоидного инфильтрата с использованием методики shaving произведено у 12 больных, резекция мочевого пузыря — у 5, резекция мочеточника с формирование уретероцистоанастомоза — у 2 (рис. 4), краевая резекция прямой кишки — у 3, передняя резекция прямой кишки — у 1, низкая передняя резекция прямой кишки и нижней трети сигмовидной кишки с наложением сигмо-ректального анастомоза и превентивной двухствольной трансверзостомой — у 1, сегментарная резекция сигмовидной кишки с формированием аппаратного анасто- моза «конец в конец» — у 1.
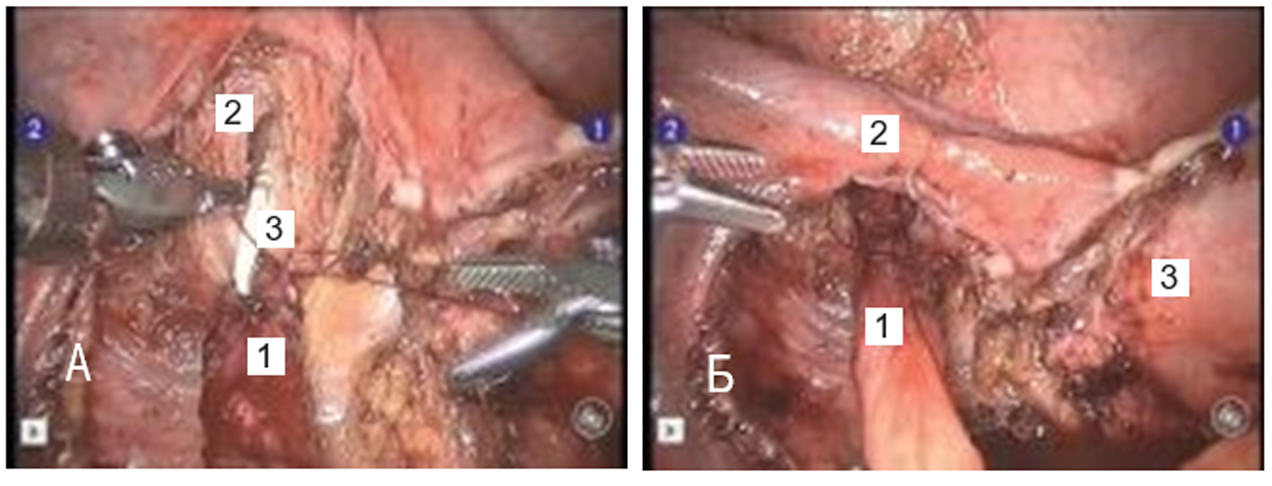 Рис. 4. Формирование уретероцистоанастомоза у больной с инфильтративным эндометриозом с вовлечением левого мочеточника. А — проведение стента из мочевого пузыря
в мочеточник: 1 — мочеточник, 2 — мочевой пузырь, 3 — стент; Б — заключительный этап операции: 1 — мочеточник, 2 — круглая связка матки, 3 — матка
Рис. 4. Формирование уретероцистоанастомоза у больной с инфильтративным эндометриозом с вовлечением левого мочеточника. А — проведение стента из мочевого пузыря
в мочеточник: 1 — мочеточник, 2 — мочевой пузырь, 3 — стент; Б — заключительный этап операции: 1 — мочеточник, 2 — круглая связка матки, 3 — маткаСложность данной категории операций определяется сильной кровоточивостью пораженных эндометриозом тканей, отсутствием четких границ инфильтрата, высоким риском ранения вовлеченных в патологический процесс органов. Во всех случаях выделяли мочеточник с целью оценки степени его вовлечения в эндометриоидный процесс и профилактики ранения. Выбор объема резекции толстой кишки определялся глубиной инвазии эндометриоза в кишечную стенку. Диссекцию очага начинали с неизмененных тканей, это позволяет повысить радикальность операции, что важно для дальнейшего прогноза течения заболевания.
Хирургическое лечение глубокого эндометриоза является вполне оправданным, но связано с высоким риском осложнений 5. Наш опыт свидетельствует о положительном влиянии радикального удаления всех очагов — уменьшаются боль и вероятность рецидива, повышаются процент наступления беременности и эффективности последующей консервативной терапии.
Средняя кровопотеря и продолжительность оперативных вмешательств с использованием робота da Vinci представлены в таблице.
Таблица. Некоторые результаты робот-ассистированных гинекологических оперативных вмешательств
| Название операции | Кол-во операций | Средняя кровопотеря, мл | Средняя длительность операции (включая время на установку оборудования), мин |
| Пангистерэктомия + тазовая лимфаденэктомия | 64 | 115,00 ± 52,97 | 186,55 ± 56,42 |
| Сакрокольпопексия | 22 | 107,14 ± 44,99 | 128,29 ± 49,98 |
| Иссечение эндометриоидного инфильтрата | 25 | 170,83 ± 125,15 | 248,75 ± 54,78 |
Следует отметить, что наличие у врача рутинного опыта работы в лапароскопической хирургии облегчает освоение данного доступа.
Осложнения в нашей практике отмечались в 2 случаях (менее 1%): ранение мочеточника при тазовой лимфаденэктомии, ранение подвздошной вены при парааортальной лимфаденэктомии. Послеоперационных осложнений и летальных исходов не было.
Произведены три конверсии. Две конверсионные лапароскопии были обусловлены недостаточным смещением точек введения троакаров вверх и ограничением манипулирования при миоме больших размеров. Третья конверсионная лапаротомия осуществлена у больной с инфильтративным эндометриозом с вовлечением прямой кишки на протяжении 7 см, что потребовало выполнения низкой передней резекции кишки с наложением разгрузочной трансферзостомии.
Длительность госпитализации составила 6,7 ± 1,2 койко-дня.
Заключение
Роботизированный хирургический комплекс позволяет квалифицированному специалисту выйти за пределы ограничений открытой хирургии и лапароскопии, благодаря внедрению ряда инженерных инноваций, улучшающих визуализацию, щадящее прецизионное манипулирование, а также эргономику хирурга.


