Увеличение стадии и индекса глисона у пациентов, перенесших робот-ассистированную радикальную простатэктомию по поводу локализованного рака предстательной железы
Цель исследования. Изучить частоту повышения стадии Т и индекса Глисона после робот-ассистированной радикальной простатэктомии (РАРП).
Материал и методы. В исследование вошли 142 пациента с локализованным раком предстательной железы, которым была выполнена стандартная нервосберегающая РАРП (44 пациента) и РАРП по разработанной нами методике с сохранением и реконструкцией перипростатических анатомических структур с сохранением (64 пациента) или без сохранения (34 пациента) сосудисто-нервных пучков полового члена.
Результаты. Во всех группах больных послеоперационный индекс Глисона оказался выше дооперационных значений (p<0,0001). При этом динамика изменения этого показателя между группами значимо не различалась (p=0,74). У 20,42% пациентов было отмечено увеличение стадии заболевания до pT3.
Выводы. Риски возможного увеличения стадии заболевания и степени злокачественности опухолевых клеток у пациентов, перенесших РАРП по поводу локализованного рака предстательной железы, должны учитываться при определении тактики ведения таких больных и при анализе ближайших онкологических результатов хирургического лечения.
Одной из важных проблем диагностики и лечения рака предстательной железы (РПЖ) остается недооценка стадии опухолевого процесса на предоперационном этапе. При выполнении робот-ассистированной радикальной простатэктомии (РАРП) пациентам с локализованным РПЖ очень низкого риска эскалация стадии заболевания после операции до pT3 и увеличение суммы баллов по шкале Глисона ≥ 7 выявляются в 35% случаев, а положительный хирургический край (ПХК) – в 16-18% случаев лечения [5,10]. В клиниках экспертного уровня частота ПХК для пациентов со стадией pT2 составляет 17,4%, со стадией pT3 – 36,9%, а частота биохимического рецидива спустя 7 лет достигает 21,27% [8]. При этом абластичность РАРП является сопоставимой с результатами открытой радикальной простатэктомии с тенденцией к более низкой частоте возникновения ПХК по сравнению с последней (12,7% и 21,6% соответственно, p=0,09) [2]. Целью настоящего исследования явилось изучение на собственном клиническом опыте частоты миграции стадии Т (классификации TNM 2016) и изменения суммы баллов по шкале Глисона (индекса Глисона) в послеоперационном периоде Р АРП, выполненной разными методиками пациентам с клинически локализованным РПЖ.
Материал и методы
В исследование вошли 142 пациента с локализованным РПЖ (стадия cT1cN0M0- cT2cN0M0), которым была выполнена РАРП как стандартной нервосберегающей техникой (группа Н-РАРП, 44 пациента), так и по разработанной нами методике с сохранением и реконструкцией перипростатических анатомических структур (сфинктер уретры, пубопростатические связки, пубо-промежностная мышца, фасция endopelvica) с сохранением (группа РАРП-А, 64 пациента) или без сохранения (группа РАРП-Б, 34 пациента) сосудисто-нервных пучков полового члена [3].
В исследование не вошли пациенты, которым операции выполнялись в период освоения методики РАРП (первые 50 случаев), пациенты с выраженной сердечно-сосудистой патологией, сахарным диабетом, предшествующими обширными операциями на органах малого таза и брюшной полости, а также пациенты, получавшие специфическое неоадъювантное лучевое или медикаментозное лечение РПЖ. Для количественных данных выполнялась проверка нормальности данных с помощью критерия Колмогорова–Смирнова. Количественные переменные, распределение которых не отличается от нормального, описаны через среднее значение и стандартную ошибку среднего. Количественные данные, распределение которых отличается от нормального, описаны при помощи медиан, 25 и 75 квартилей. Динамика для нормально распределенных данных исследована при помощи критерия АNOVA Repeated. Для данных, распределение которых отличается от нормального, применялся критерий Вилкоксона (по двум временным точкам) или критерий Фридмана (по семи временным точкам). Динамика исследовалась во всей совокупности больных и в каждой группе по отдельности.
Результаты
На рис. 1 приведены данные об уровне ПСА сыворотки крови в исследованных группах больных. Минимальный уровень ПСА сыворотки крови у пациентов групп Н-РАРП, РАРП-А и РАРП-Б составил 3,7 нг/мл, 0,54 нг/мл и 8,8 нг/мл соответственно, а максимальный – 70 нг/мл, 48 нг/мл и 23 нг/мл. Медиана значений ПСА сыворотки крови в группах составила соответственно 9 (6,5;13) нг/мл, 8,4 (6,6;13,6) нг/мл и 13,24 (11,1;19) нг/мл (группы однородны по уровню ПСА, критерий Краскела–Уоллиса, р=0,08) (рис. 1).
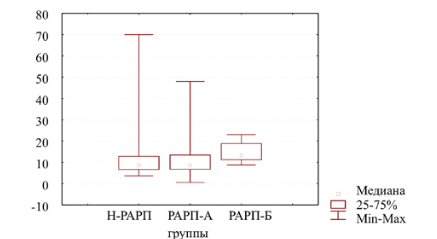 Рис. 1. Уровень ПСА (нг/мл) сыворотки крови в группах. Примечание. Различия между группами статистически не значимы, p=0,08
Рис. 1. Уровень ПСА (нг/мл) сыворотки крови в группах. Примечание. Различия между группами статистически не значимы, p=0,08
Исходная сумма баллов по шкале Глисона (установленная на основании результатов мультифокальной биопсии предстательной железы у всех пациентов) в группах Н-РАРП, РАРП-А и РАРП-Б составила соответственно 6 (6;7) бал- лов, 6 (6;6) баллов и 7 (6;7) баллов (р=0,21, рис. 2). Как следует из рис. 2, минимальное значение показателя в группах составило соответственно 5 баллов, 2 балла и 5 баллов для Н-РАРП, РАРП- А и РАРП-Б, а максимальное значение во всех группах было 8 баллов.
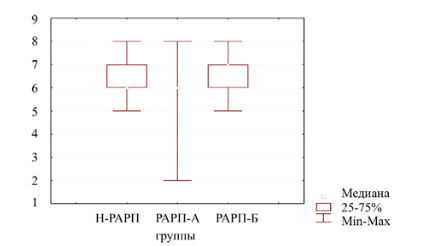 Рис. 2. Сумма баллов по шкале Глисона до операции. Примечание. Различия между группами статистически не значимы, p=0,21
Рис. 2. Сумма баллов по шкале Глисона до операции. Примечание. Различия между группами статистически не значимы, p=0,21
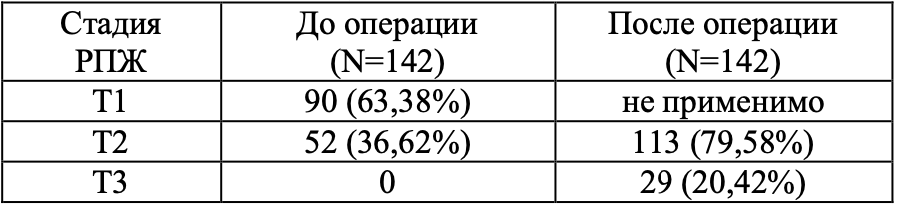
В табл. 1 представлены данные по стадиям заболевания у пациентов исследованных групп. Во всех группах у больных была диагностирована локализованная форма РПЖ (T1- T2N0M0). Стадия cT1 была установлена у 90 (63,38%), сТ2 – у 52 (36,62%) пациентов. Стадирование осуществляли на основании данных гистологического исследования материала биопсии тканей предстательной железы, данных МРТ органов малого таза, остеосцинтиграфии и рентгенографии грудной клетки.
Таблица 1. Распределение больных РПЖ по стадии болезни, Т (классификация TNM 2016)
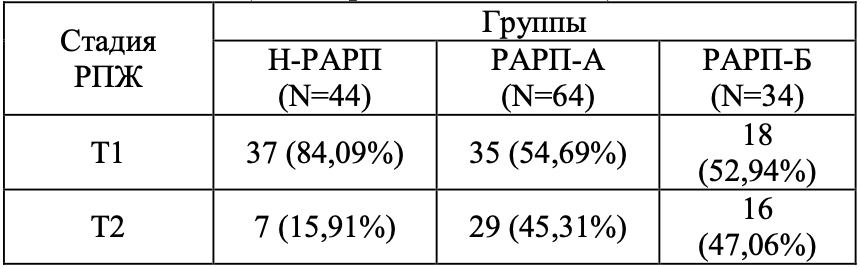
У всех пациентов было выполнено послеоперационное гистологическое исследование операционного материала. При исследовании препарата предстательной железы во всех группах больных показатель суммы баллов по шкале Глисона оказался выше дооперационных значений. В табл. 2 приведены медиана, нижний и верхний квартили показателя суммы баллов по шкале Глисона в исследованных группах больных до и после операции.
Таблица 2. Сумма баллов по шкале Глисона до и после операции
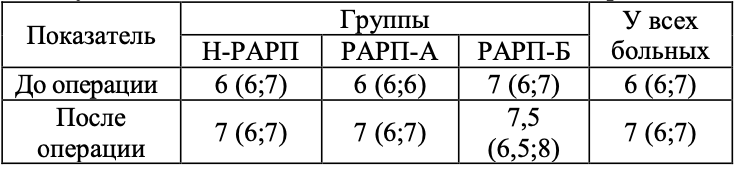
Максимальные значения показателя суммы баллов по шкале Глисона после операции составили 10 баллов в группе Н-РАРП и 9 баллов в группах РАРП-А и РАРП-Б. Увеличение показателя суммы баллов по шкале Глисона было статистически значимо относительно исходных значений во всех исследованных группах (p<0,0001). При этом динамика изменения этого показателя между группами значимо не различалась (p= 0,74) (рис. 3).
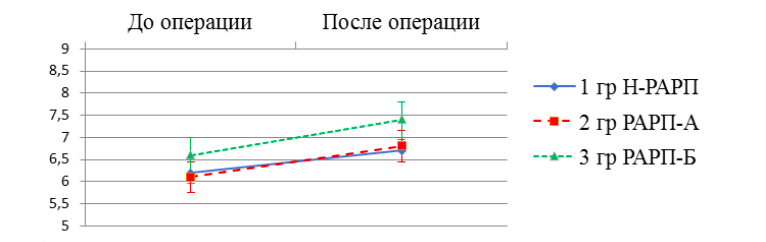 Рис. 3. Динамика показателя суммы баллов по шкале Глисона. Примечание. Различия в динамике по группам статистически не значимы, p=0,74
Рис. 3. Динамика показателя суммы баллов по шкале Глисона. Примечание. Различия в динамике по группам статистически не значимы, p=0,74
Частота встречаемости положительного хирургического края (ПХК) в группах больных значимо не различалась и составила 14,29%, 17,19% и 14,71% соответственно для Н-Р АРП, Р АРП-А и Р АРП-Б (p=0,82). Было выявлено различие в стадиях РПЖ до и после операции (табл. 3): у 20,42% пациентов была отмечена эскалация стадии заболевания до местно-распространенного процесса – стадии T3. Биохимический рецидив за весь период наблюдения был выявлен у 6% пациентов, при этом от прогрессии РПЖ за весь период наблюдения не умер ни один больной.
Таблица 3. Различия в клинической и патологической стадиях РПЖ (TNM, 2016 г.)
Обсуждение
В нашей работе недостадирование стадии pT3 составило более 20%, что соотносит- ся с данными других исследователей. Так, в исследовании Е.И. Велиева и соавт. при клинически локализованном РПЖ стадия pT3aN0 была выявлена у 13,5% пациентов, pT3b-4N0 – у 7,4% [1]. Нами было установлено значимое увеличение средних значений суммы баллов по шкале Глисона, что также соотносится с имеющимися литературными данными [1,6,9]. Отсутствие же статистически значимых различий в динамике показателя между группами позволяет сделать вывод об их сопоставимости. В исследовании C. D’Elia и соавт. у 46,7% пациентов с клиническим значением суммы баллов по шкале Глисона от 4 до 6 баллов при патологическом исследовании удаленной простаты значение было повышено до 3+4=7 баллов, а у 5,3% – до 4+3=7 баллов. Также у 39,7% была выявлена более высокая стадия РПЖ [6]. В другом исследовании миграция индекса Глисона после операции в сторону увеличения наблюдалась у 17,5% пациентов, в сторону уменьшения – у 7,6% [1].
В нашем исследовании частота ПХК в среднем в группах составила 15,4%, при этом частота ятрогенного ПХК, т.е. такого, когда линия отсечения прошла внутри капсулы железы, составив 1,4%. Такое разделение причин возникновения ПХК, на наш взгляд, важно, поскольку в случае, если клиническая стадия опухоли соответствует cT2, а при гистологическом исследовании определяется pT3a, то ситуация объясняется ошибкой стадирования. При этом хирург выполнял вмешательство, ориентируясь на показатели ПСА в сыворотке крови, суммы баллов по шкале Глисона и клиническую стадию заболевания, выполняя диссекцию вплотную к предстательной железе для максимального сохранения сосудисто-нервных пучков полового члена. Другая ситуация складывается, когда хирург оперирует больного с клинически локализованным РПЖ и патологоанатомический диагноз не расходится с клиническими данными (pT2), однако диагностируют ПХК. Это означает, что хирург допустил ошибку, выполнив диссекцию в неверном слое, и у таких пациентов вероятность развития биохимического рецидива возрастает [7]. Наличие ПХК может оказывать влияние на возникновение клинического рецидива заболевания у 15% пациентов, особенно в тех случаях, когда выявлены высокая стадия опухоли или низкодифференцированная опухоль [1].
Таким образом, зачастую мы оперируем больных с более агрессивным течением опухолевого процесса, чем предполагается на дооперационном этапе и/или местно-распространенным процессом. Риск возникновения ПХК после РАРП должен быть оценен заблаговременно, а частичное билатеральное или унилатеральное сохранение сосудисто-нервных пучков в ходе вмешательства может обеспечить более высокую абластичность процедуры. При этом достичь раннего восстановления континенции можно даже у тех больных, кому не выполнялось сохранение сосудисто-нервных пучков [3]. Вероятность недооценки стадии и степени злокачественности опухоли у значительного числа пациентов с локализованным РПЖ низкого риска также должна учитываться при выборе тактики активного наблюдения таких больных.
Заключение
Риски возможного повышения стадии заболевания при патологическом исследовании удаленного препарата предстательной железы и увеличения степени злокачественности опухолевых клеток у пациентов с локализованным РПЖ должны учитываться при определении тактики ведения таких больных и анализе ближайших результатов хирургического лечения.
Сведения об авторах статьи
- Мосоян Мкртич Семенович – д.м.н., профессор кафедры урологии с курсом урологии с клиникой ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России, завкафедрой урологии с курсом роботической хирургии, руководитель центра роботической хирургии; ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России. Адрес: г. Санкт-Петербург, ул. Аккуратова, 2. E-mail: moso03@yandex.ru.
- Ильин Дмитрий Михайлович – врач-уролог СПб ГБУЗ «Городская Мариинская больница». Адрес: г. Санкт-Петербург, Литейный пр., 56. E-mail: melker@mail.ru.








