Торакобедренное бифуркационное шунтирование с использованием робототехники
Аннотация
Введение. Торакобифеморальное шунтирование при окклюзии аортофеморального сегмента является вариантом выбора метода лечения пациентов при невозможности проведения традиционного аортофеморального шунтирования. Использование робот-ассистированных технологий при формировании проксимального анастомоза позволяет уменьшить травматичность операционного доступа и улучшить результаты оперативного вмешательства. В статье приводится клиническое наблюдение пациента с окклюзией аорто-подвздошного сегмента и тотальным кальцинозом инфраренального отдела аорты, которому выполнено торакобедренное бифуркационное шунтирование с применением робототехники.
Заключение. Использование в сосудистой хирургии современных технологий позволяет уменьшить травматизацию, минимизировать влияние человеческого фактора, улучшить визуализацию и свободу движений, при этом сократить восстановительный период пациента и время его нахождения в стационаре.
Введение
Атеросклеротические поражения брюшной части аорты и периферических артерий — наиболее распространенная патология сердечно-сосудистой системы Эпидемиологические многоцентровые исследования, проведенные в конце XX в — начале XXI в., показывают, что в общей популяции экономически развитых стран распространенность периферического атеросклероза достаточно высока и составляет 3–10%, а среди лиц старше 70 лет достигает 15–20% [1].
Аортобифеморальное шунтирование остается «золотым стандартом» лечения пациентов с тяжелым атеросклеротическим заболеванием или полной окклюзией инфраренального отдела аорты и подвздошных артерий В случаях тотального кальциноза брюшной части аорты, а также спаечного процесса в полости живота, при тромбозе и инфекции предшествующих реконструкций инфраренальной аорты и других внутрибрюшных патологий, не позволяющих провести стандартную реваскуляризацию нижних конечностей (НК), методом выбора может служить торакофеморальное шунтирование [2]. Выполнение открытых оперативных вмешательств связано с высоким риском периоперационных осложнений и длительным реабилитационным периодом [3].
Активное внедрение эндовидеохирургии с использованием робототехники улучшает результаты хирургических вмешательств: минимизирует травматизацию тканей и сокращает сроки операций, способствует восстановлению пациентов в более короткие сроки.
Клинический случай
Пациент З., 68 лет, поступил в отделение сосудистой хирургии Научно-исследовательского института — Краевой клинической больницы № 1 имени профессора С. В. Очаповского г. Краснодара в июне 2022 г. с жалобами на боль в икроножных мышцах в покое, сухие некрозы 1-го пальца стопы левой НК, боли в икроножных мышцах правой НК при прохождении дистанции до 10 м. Считает себя больным в течение 5 лет. Последний месяц отмечает ухудшение состояния, нарушение сна ввиду выраженного болевого синдрома.
Из анамнеза жизни: больной наблюдается у эндокринолога по поводу сахарного диабета 2 типа, болеет более 20 лет, получает инсулинотерапию.
При выполнении мультиспиральной компьютерной томографии (МСКТ) с внутривенным контрастированием было выявлено атеросклеротическое поражение аорты и ее ветвей, тотальный кальциноз инфраренального отдела аорты, окклюзия терминального отдела аорты, обеих общих подвздошных артерий, наружных подвздошных артерий, окклюзия поверхностных бедренных артерий (БА) обеих НК.
По данным ангиографии подтверждается уровень окклюзии: глубокая бедренная, подколенные и берцовые артерии определяются проходимыми На основании данных пациенту выставлен клинический диагноз: Атеросклероз. Синдром Лериша. Окклюзия терминального отдела аорты, обеих общих наружных подвздошных артерий, окклюзия поверхностных БА обеих НК. Хроническая артериальная недостаточность III степени обеих НК.
Техника операции. После введения общей анестезии и установки двухпросветной эндотрахеальной трубки пациента разместили на правом боку с отведенной вправо левой рукой. Первым этапом латерально выполнили разрез в проекции БА с обходом феморальных лимфоузлов. Последовательно выделены и взяты на держалки общая, поверхностная и глубокая БА обеих НК Поверхностные БА обеих НК несжимаемые, кальцинированы, глубокие БА мягкие, сжимаемые Далее выполнен люмботомный доступ слева Брюшной мешок оттеснен кверху и медиально Осуществлена ревизия забрюшинного пространства, диафрагмы. Бифуркационный протез из полиэстера проведен ретроперитонеально по ходу подвздошных артерий в дистальном направлении слева и справа, бранши протеза проведены под паховой связкой к БА.
Следующим этапом устанавливались троакары в грудную область. На уровне задней подмышечной линии в левой грудной области в VI межреберье установлен видеооптический троакар 8 мм В троакар введен лапараскоп. При ревизии доли легкого воздушны, в акте дыхания не учувствуют ввиду однолегочной вентиляции, париетальная и висцеральная плевра без патологии Имеется единичный спаечный процесс в верхней части доли легкого. Далее медиальнее видеооптического троакара на уровне средней подмышечной линии в VI межреберье установлен троакар 8 мм для 2 роботического манипулятора По передней подмышечной линии в V межреберье установлен троакар 8 мм для 1 роботического манипулятора По лопаточной линии в V межреберье установлен троакар 8 мм для 4 роботического манипулятора. Далее выполнена миниторакотомия длиной до 3 см в VIII межреберье между видеооптическим троакаром и 4 роботическим манипулятором для аортального зажима. Проведена миниторакотомия длиной до 3 см в VII межреберье между видеооптическим троакаром и 2 роботическим манипулятором для аспиратора. По задней подмышечной линии между видеооптическим троакаром и 4 роботическим манипулятором в IV межреберье выполнена миниторакотомия длиной до 4 см для аортального зажима (рис 1).
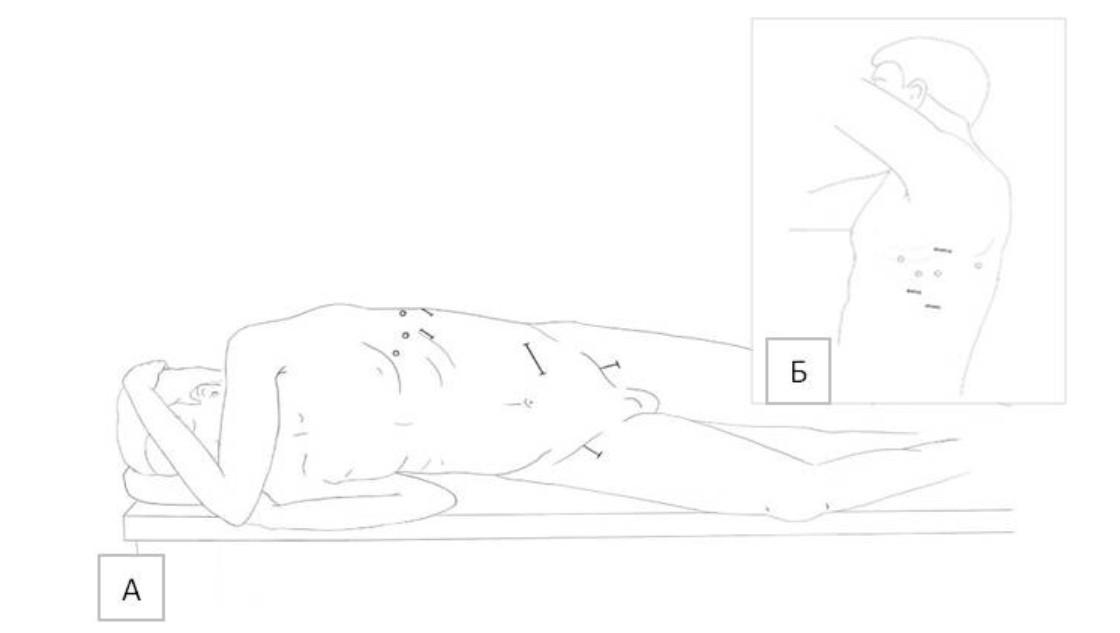 Рис. 1. Схема положения пациента на операционном столе (А) и расположения троакаров и открытых хирургических доступов (Б).
Рис. 1. Схема положения пациента на операционном столе (А) и расположения троакаров и открытых хирургических доступов (Б).
Манипуляторы роботической установки Da Vinci Xi фиксированы, с помощью роботических рук иссечен единичный спаечный процесс в верхней доле легкого. Выделен дистальный отдел нисходящей грудной аорты В сухожильной части диафрагмы сформировано отверстие с целью проведения синтетического протеза Протез проведен по левому боковому каналу и далее в левую плевральную полость через сформированное отверстие в диафрагме. Введено 2500 единиц действия гепарина натрия внутривенно Для бокового отжатия грудного отдела нисходящей части аорты в плевральную полость через миниторакотомные раны с помощью 1 и 3 ассистентской руки заведены 2 изогнутых аортальных зажима Сатинского. Зажимы наложены навстречу друг другу Осуществлено боковое отжатие аорты Проведена продольная аортотомия Непрерывным швом нитью пролен 4 0 по типу «конец-в-бок» сформирован проксимальный анастомоз между синтетическим протезом и аортой. Поочередно сняты зажимы с аорты, осуществлена адаптация анастомоза (рис 2).
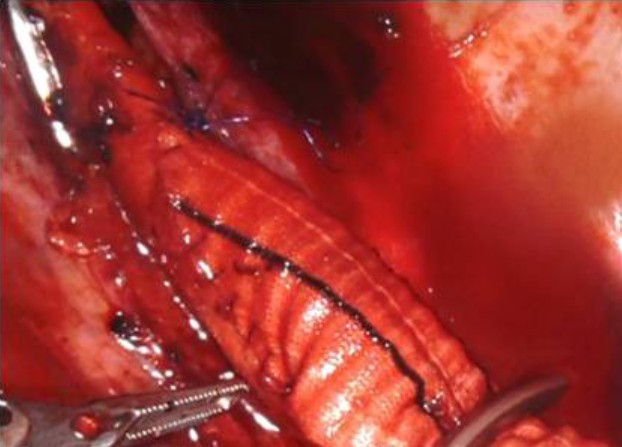 Рис. 2. Вид на сформированный проксимальный анастомоз между синтетическим протезом и аортой. Адаптация проксимального анастомоза между нисходящей частью грудной аорты и синтетическим протезом.
Рис. 2. Вид на сформированный проксимальный анастомоз между синтетическим протезом и аортой. Адаптация проксимального анастомоза между нисходящей частью грудной аорты и синтетическим протезом.
Через 2 роботизированный порт под контролем лапароскопа выведен плевральный дренаж. Роботические манипуляторы вместе с торакальными портами удалены. Следующим этапом сформированы дистальные анастомозы между браншами протеза и общими БА с переходом на глубокие БА по типу «конец-в-бок» непрерывным швом нитью пролен 5.0. Проведена адаптация анастомозов, артерии пульсируют в ране Осуществлено дренирование ран на бедрах по Редону. Подключен плевральный дренаж. Раны ушиты.
Длительность оперативного вмешательства составила 310 мин. Время бокового отжатия аорты — 36 мин., время формирования проксимального анастомоза с использованием робототехники — 31 мин. Объем кровопотери составил около 350 мл. Пациент был экстубирован через 20 мин после окончания операции на операционном столе, переведен в отделение реанимации и интенсивной терапии.
Послеоперационный период больного протекал без особенностей и осложнений Ишемия НК купирована. На 2 сутки после операции пациент переведен в общую палату Через 1 сутки после операции — самостоятельный стул. С целью послеоперационного контроля на 3 сутки удалены дренажи (рис. 3) и выполнена МСКТ с внутривенным контрастированием с шагом 1 мм Конструкция проходима, препятствий для кровотока нет (рис. 4).
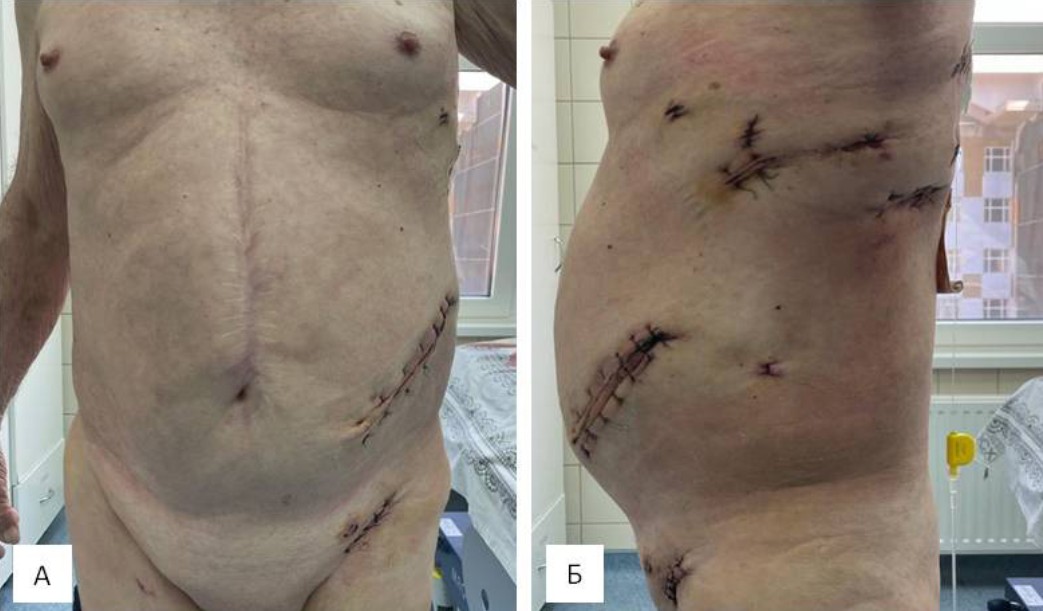 Рис. 3. Послеоперационные раны после удаления дренажей (3 сутки): А — вид спереди, Б — вид сбоку.
Рис. 3. Послеоперационные раны после удаления дренажей (3 сутки): А — вид спереди, Б — вид сбоку.
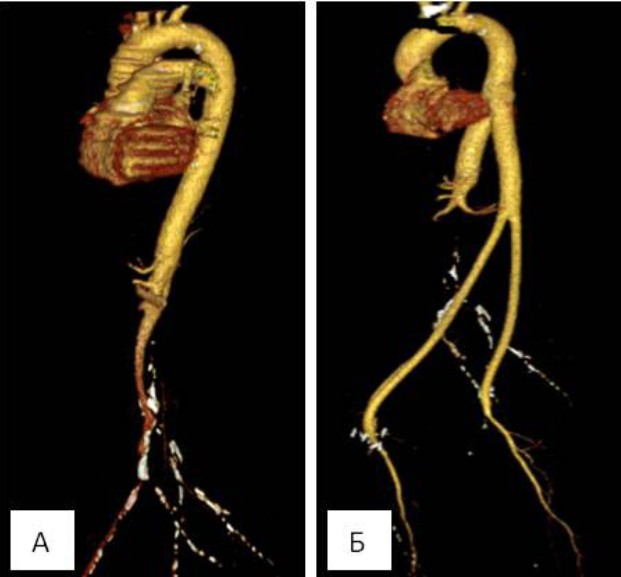 Рис. 4. Трехмерная реконструкция мультиспиральной компьютерной томографии с внутривенным контрастированием: А — до оперативного вмешательства, Б — после оперативного вмешательства.
Рис. 4. Трехмерная реконструкция мультиспиральной компьютерной томографии с внутривенным контрастированием: А — до оперативного вмешательства, Б — после оперативного вмешательства.
Обсуждение
Робот-ассистированная хирургия — одна из самых совершенных на сегодняшний день технологий малоинвазивной эндовидеохирургии. Высокая точность и свобода движений, трехмерное изображение, минимизация вмешательства и кровопотери, укороченный период реабилитации пациентов — факторы, которые позволяют активно внедрять «роботические» операции в различные специальности Короткая кривая обучения способствует применению роботических хирургических систем в сосудистой хирургии при выполнении оперативных вмешательств на магистральных сосудах с минимизацией травматичности хирургических доступов, что делает перспективным использование робототехники при сложных реконструкциях на аортофеморальном сегменте [4–7].
В современной практике при окклюзии аортоподвздошного сегмента традиционной реконструктивной операцией является аортобифеморальное шунтирование, которое имеет наиболее долгосрочные результаты проходимости. В группе больных высокого риска и для пациентов, у которых обычная реконструктивная операция не представляется возможной, альтернативным вариантов является торакобифеморальное шунтирование.
У разных авторов техника выполнения торакобифеморального шунтирования отличается В большинстве случаев используется переднебоковая торакотомия с задним туннелем под левой ножкой диафрагмы. Трансплантат подводится к левой паховой области, а затем одна бранша шунта туннелируется в правую бедренную область [8].
Выполнение стандартной переднебоковой торакотомии для выделения нисходящей части грудного отдела аорты и формирования проксимального анастомоза является очень травматичным доступом и связано с высоким риском повреждения реберного каркаса и длительными сроками послеоперационной реабилитации. Стандартное открытое оперативное лечение у пациентов с ожирением, бочкообразной грудной клеткой может сопровождаться высокими техническими сложностями. Применение робот-ассистированных технологий при формировании проксимального анастомоза позволяет уменьшить травматизацию операционной раны, кровопотерю и улучшить восстановительный период больных.
Одним из минусов является возможность столкновения манипуляторов робота с лапароскопическими инструментами, что может привести к снятию аортального зажима Успехом оперативного вмешательства является взаимосвязь между ассистентом хирурга за столом и хирургом за консолью. Следует избегать быстрых, внезапных перемещений инструментов Кроме того, важна правильная установка троакара с достаточным пространством между роботизированными и лапароскопическими инструментами. Роботизированная система не обеспечивает тактильной обратной связи, поэтому необходимо соблюдать осторожность при взаимодействии с тканями тела, швами и протезным материалом. Для помощи во время роботизированной хирургии при выполнении быстрой конверсии, когда это необходимо, требуется присутствие опытных хирургов в операционной. Кроме того, важно учитывать затраты на роботизированную систему, обслуживание и инструменты [9].
Заключение
Использование в сосудистой хирургии современных технологий позволяет уменьшить травматизацию, минимизировать влияние человеческого фактора, улучшить визуализацию и свободу движений, при этом сократить восстановительный период пациента и время его нахождения в стационаре.
Применение робототехники способствует улучшению реабилитации пациентов и уменьшению риска послеоперационных осложнений без увеличения объема оперативного вмешательства и времени пережатия сосудов, что делает перспективным использование робот-ассистированных технологий при выполнении сложных реконструктивных вмешательств.
Дополнительно
Финансирование. Авторы заявляют об отсутствии внешнего финансирования при проведении исследования.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Согласие на публикацию. В статье использованы обезличенные клинические данные пациента в соответствии с подписанным им добровольным информированным согласием.
Вклад авторов: Бутаев С. Р., Виноградов Р. А. — концепция; Бахишев Т. Э., Хангерееев Г. А. — сбор и обработка материала; Закеряев А. Б., Бахишев Т. Э., Ерастова А. В. — написание текста; Порханов В. А., Виноградов Р. А., Барышев А. Г. — редактирование.
Авторы подтверждают соответствие своего авторства международным критериям ICMJE (все авторы внесли существенный вклад в разработку концепции, подготовку статьи, прочли и одобрили финальную версию перед публикацией).


