Факторы риска недержания мочи у пациентов, перенесших радикальную робот-ассистированную простатэктомию
Аннотация
Введение. Рак предстательной железы (РПЖ) относится к одним из самым распространённых онкологических заболеваний, и тактика его лечения напрямую зависит от стадии. «Золотым» стандартом при локализованном раке простаты является выполнение оперативного вмешательства в объёме радикальной робот-ассистированной простатэктомии (РАРПЭ). Пациенты часто имеют высокие требования к операции и обеспокоены развитием постоперационных осложнений. Одним из наиболее частых функциональных осложнений после данной операции является недержание мочи (НМ), механизм формирования которого до конца не изучен. В клинических исследованиях описано множество предрасполагающих к инконтинеции факторов, однако полученные результаты часто оказываются противоречивы, что требует более глубокого изучения вопроса.
Цель исследования. Выявить предрасполагающие факторы недержания мочи у пациентов, перенесших радикальную робот-ассистированную простатэктомию.
Материалы и методы. Были проанализированы результаты поиска по научным базам данных PubMed, Medline, Web of Science, Embase, Cochrane Library and PEDro, Wang-fang Database и CNKI, Edline по запросам «робот-ассистированная простатэктомия», «радикальная простатэктомия», «инконтиненция», «предикторы», «недержание мочи».
Результаты. Изучены предрасполагающие факторы НМ после РАРПЭ. В обзоре подробно рассмотрены и проиллюстрированы все известные предрасполагающие факторы НМ и показана противоречивость полученных данных у разных исследователей, что лишний раз подчёркивает необходимость дальнейшего изучения этого вопроса.
Заключение. Несмотря на длительную историю изучения постоперационных осложнений РАРПЭ, до сих пор не получено достоверных и непротиворечивых данных о всех рисках НМ после РАРПЭ, поэтому в данном литературном обзоре проанализированы и собраны результаты новейших исследований последних лет.
Ключевые слова: рак предстательной железы; радикальная простатэктомия; робот-ассистированная простатэктомия; инконтиненция; предикторы; недержание мочи
Финансирование. Исследование не имело спонсорской поддержки.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Введение
Рак предстательной железы (РПЖ) является одним из самых распространённых заболеваний мужчин во всем мире [1]. Радикальная простатэктомия (РПЭ) является «золотым» стандартом лечения локализованного РПЖ [2, 3]. В настоящее время всё чаще операция выполняется робот-ассистированно (РАРПЭ), что имеет ряд преимуществ перед «классической» позадилонной и лапароскопической простатэктомией. К ним относят меньший объём кровопотери, менее продолжительный период дренирования мочевого пузыря уретральным катетером, снижение потребности в использовании обезболивающих средств в постоперационном периоде, более быструю реабилитацию пациентов [4 – 10]. Наряду с хорошим онкологическим результатом важен и функциональный исход операции, заключающийся в восстановлении эректильной функции и удержании мочи. Недержание мочи (НМ) — это патологическое состояние, характеризующееся любым непроизвольным выделением мочи из уретры [11]. Безусловно, качество жизни у пациентов с недержанием мочи после РПЭ снижается, этот факт отмечает до 87% прооперированных больных [12]. С данным осложнением сталкивается от 2 до 65% прооперированных мужчин [13, 14]. Сегодня исследуются различные факторы, увеличивающие риск появления недержания мочи после РПЭ. Их можно условно объединить в разные группы: предоперационные, интраоперационные и постоперационные. В данной статье мы рассматриваем предоперационные факторы риска.
Цель исследования: выявить предрасполагающие факторы недержания мочи у пациентов, перенёсших радикальную робот-ассистированную простатэктомию.
Алгоритм литературного поиска
Были проанализированы результаты поиска по научным базам данных PubMed, Medline, Web of Science, Embase, Cochrane Library and PEDro, Wang-fang Database и CNKI, Edline по запросам «роботассистированная простатэктомия», «радикальная простатэктомия», «инконтиненция», «предикторы», «недержание мочи». В результате проведённого поиска выявлены следующие предрасполагающие факторы: возраст пациента, индекс массы тела, сопутствующие заболевания, анатомические особенности, функциональные изменения мочевого пузыря, перенесённые операции.
Возраст пациента
Существует множество публикаций, доказывающих взаимосвязь возраста прооперированного пациента с развитием НМ в послеоперационном периоде. Чем старше мужчина, тем больший объём имеет предстательная железа, к тому же зачастую возникают и функциональные изменения в мочевом пузыре. Поэтому у возрастных больных выраженность симптомов нижних мочевых путей значительнее выше, чем у более молодых пациентов. В исследовании G. Novara et al. установили, что мужчины, у которых восстановилось удержание мочи спустя 1 год после операции, были значительно моложе тех, кто по-прежнему страдал НМ [10]. Следует отметить, что конкретное число лет пациента до сих пор остаётся предметом дискуссий. По данным одних исследований, пациенты в возрасте старше 70 лет чаще встречаются с недержанием мочи в постоперационном периоде и имеют более долгий период восстановления [15, 16]. В работе K. Matsushita et al., включавшей 2849 больных, было выявлено, что у пациентов старшей возрастной группы через 6 и 12 месяцев после простатэктомии сохранялось недержание мочи [17]. Существует ряд исследований, где подобной связи выявлено не было. К примеру, в исследовании Y. Kadono et al., включавшем 111 пациентов, влияния возраста на восстановление удержания мочи выявлено не было [18].
Индекс массы тела
Индекс массы тела (ИМТ) — это величина, позволяющая оценить степень соответствия роста человека к весу и рассчитывается по формуле: m (масса тела в килограммах) / h2 (рост в метрах). Ожирением страдают люди с ИМТ от 30 кг/м2 и более. Установлено, что у больных с ожирением восстановление как эректильной функции, так и удержания мочи протекает медленнее, чем у пациентов с нормальным показателем ИМТ [19]. К примеру, в работе K. Y. Wolin et al. пришли к тому, что НМ после простатэктомии чаще встречалось у мужчин с ожирением (ИМТ > 30 кг/м2), которые закономерно вели малоактивный образ жизни [20]. A. L. Wiltz et al. обнаружили, что среди 945 пациентов, перенёсших РАРПЭ, результаты удержания мочи в течение 2 лет после операции были значительно хуже у пациентов с ожирением. Тем не менее, и здесь ситуация не такая однозначная. Нельзя не отметить исследования Y. Kadono et al. или E. I. Hsu et al., где связи между ИМТ и сроком восстановления удержания мочи установлено не было [18, 21].
Сопутствующие заболевания
Существуют работы, в которых описывается более продолжительное восстановление функции удержания мочи пациентов с метаболическим синдромом. Метаболический синдром — симптомокомплекс, включающий ожирение по абдоминальному типу, инсулинорезистентность, гипергликемию, дислипидемию и артериальную гипертензию. К примеру, через 3 месяца после перенесённой операции больные с данной патологией попрежнему страдали недержанием мочи по сравнению с теми, кто не имел этого заболевания. В исследовании M. Nishikawa et al., включавшем 302 больных, у 10,2% мужчин в анамнезе упоминался метаболический синдром. Было установлено, что в течение первых 3 месяцев после РАРПЭ эта группа пациентов в большей степени страдала НМ [22].
Анатомические особенности
В некоторых публикациях отмечается корреляция индивидуальных особенностей различных структур и образований малого таза с постпростаткэтомической инконтиненцей. Выявлено, что у пациентов с предстательной железой менее 40 см3 уже в течение первого месяца после операции восстанавливается удержание мочи [23]. В другом исследовании у пациентов с объёмом предстательной железы менее 30 см3 недержания мочи в постоперационном периоде не отмечались вовсе [24]. В работе J. Boczko et al., включавшей более 350 мужчин, которые перенесли экстраперитонеальную РАРПЭ, был сделан вывод о том, что пороговым является показатель в 75 мл; больные с размером простаты < 75 мл демонстрировали лучшие функциональные результаты в течение полугода после операции [25]. B. R. Konety et al. в ещё более масштабном исследовании приводили данные о том, что пациенты с объёмом простаты < 50 см3 реже сталкивались с инконтиненцией через 6 и 12 месяцев после перенесенной РПЭ [26]. Безусловно, есть и альтернативная точка зрения. Существуют исследования, где связь между объёмом предстательной железы и недержанием мочи после операции не была выявлена [18, 27].
Возникновение инконтиненции у пациентов с бо́льшим объёмом предстательной железы является следствием резекции более обширной части уретры в ходе операции, что в свою очередь приводит к уменьшению её общей протяжённости и, как следствие, меньшей длине мембранозного отдела уретры, о чем и пойдёт речь далее.
Значительную роль в формировании удержания мочи в постоперационном периоде имеет длина мембранозного отдела уретры: чем это значение больше, тем быстрее у больного восстанавливается континенция [28]. Эти данные были получены в результате оценки снимков МРТ органов малого таза с контрастированием у пациентов до операции и оценки функции удержания мочи после. Следует отметить, что работ такого типа достаточно много. Была предложена специальная классификация (Lee type A – D) по расположению верхушки предстательной железы относительно мембранозного отдела уретры:
- Тype А — верхушка предстательной железы окружает мембранозный отдел уретры спереди и сзади;
- Тype B — верхушка предстательной железы окружает мембранозный отдел уретры спереди;
- Type C — верхушка предстательной железы окружает мембранозный отдел уретры сзади;
- Type D — верхушка предстательной железы не охватывает мембранозный отдел уретры (рис. 1) [29].
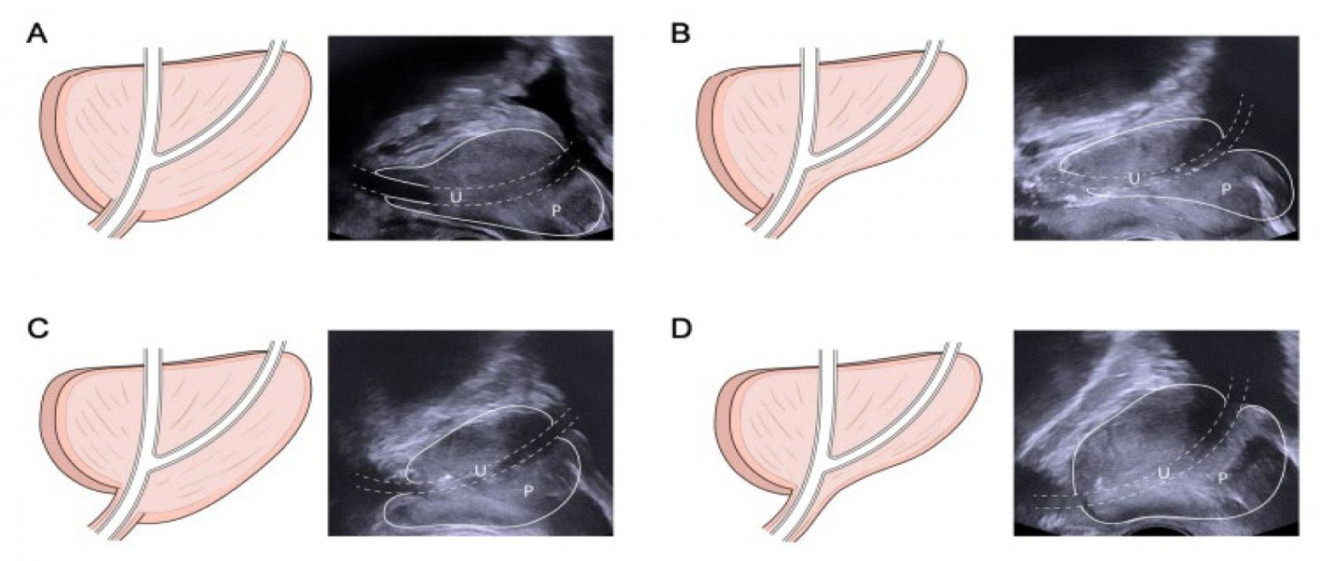 Рисунок 1. Типы предстательной железы по классификации Lee (A – D) [29]
Рисунок 1. Типы предстательной железы по классификации Lee (A – D) [29]
В соответствии с данной классификацией больные с формой предстательной железы типа C и D начинают удерживать мочу в самые ранние сроки после операции, что доказано в одном из исследований 2021 года [30].
В исследовании L. Ngueyen et al. выявили, что длина уретрального сфинктера до операции в среднем составляет 14 мм. Восстановление континенции через 1 год после операции у пациентов с длиной уретры более 12 мм наблюдалось в 89% случаев по сравнению с 77% пациентов со значением менее 12 мм. К тому же, в первой группе отмечалось более быстрое формирование удержания мочи в целом. Бо́льшая длина сфинктера как до РПЭ, так и сохранившаяся после операции, также играла свою положительную роль в континенции пациентов [31]. К схожему заключению пришли и P. Paparel et al., продемонстрировав в своей работе, что пред- и постоперационная длина мембранозного отдела уретры и степень её резекции во время РПЭ коррелировали со сроком полного восстановления континенции и степенью удержания мочи в ранние сроки [32]. В исследовании K. Matsushita et al., включавшем 2849 пациентов, установлено, что у мужчин с достаточной длиной мембранозного отдела уретры удержание мочи через 6 и 12 месяцев после операции было гораздо лучше по сравнению с контрольной группой [33].
С другой стороны, J. F. Borin et al. не выявили достоверного различия между временем восстановления континенции и более радикальной диссекцией ткани в области верхушки простаты для избежания положительного хирургического края. Отмечено, что частота положительного хирургического края снизилась с 13,0 до 5,5% при выполнении более радикальной резекции уретры. При этом значимой разницы инконтиненции у пациентов при диссекции на 1 см ниже или выше мочеполовой диафрагмы установлено не было. Более того, не выявлена корреляция между континенцией и длиной оставшейся культи уретры после РПЭ [34].
Существуют исследования, в которых оценивается вклад в удержание мочи иных структур малого таза. К примеру, в некоторых работах указывают на роль толщины стенки уретры по данным МРТ. Отмечалось, что чем меньше это значение, тем быстрее происходит восстановление удержания мочи [28]. В этом исследовании также оценивалось влияние различных параметров на формирование удержания мочи после РПЭ: объём предстательной железы (PV), длина мембранозного отдела уретры (MUL) (значение которых описано ранее), мышца, поднимающая задний проход (LAM), размер внутренней запирательной мышцы (OIM), отношение m. levator ani к объёму простаты (LAM/PV), объём уретры (VU). На рисунке 2 приведён пример измерений описанных структур.
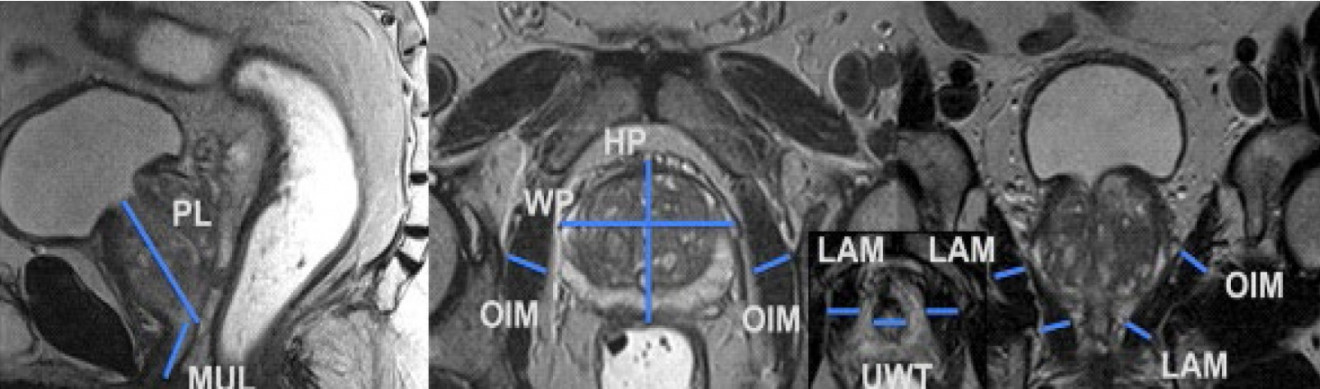 Рисунок 2. Структуры малого таза (описание в тексте) [28]
Рисунок 2. Структуры малого таза (описание в тексте) [28]
В исследовании C. von Bodman et al. очередной раз подтверждается роль длины уретры в удержании мочи, но при этом указывается на значение объёма уретры и взаимоотношение m. levator ani к простате. Также было установлено, что бо́льшие расстояния между внутренним и внешним листками леваторов тесно связаны со снижением вероятности восстановления континенции через 6 и 12 месяцев, однако для других временных точек подобной корреляции не выявлено [35].
В исследовании C. W. Jeong et al. присутствует несколько примечательных моментов: безусловно подтверждается влияние длины мембранозного отдела уретры и объёма предстательной железы на постпростатэктомическую инконтиненцию, составлена номограмма по предрасполагающим факторам недержания мочи и, что не было описано в других подобных работах, влияние объёма дорзального комплекса на удержание мочи. По данным исследователей, у больных с бо́льшим объёмом дорзального комплекса (2,3 – 2,8 см3) удержание мочи происходило существенно быстрее [36].
Функциональные изменения мочевого пузыря
Встречаются работы, в которых обнаруживается связь между гиперактивным мочевым пузырём и временем восстановления удержания мочи после РПЭ. Гиперактивный мочевой пузырь — симптомокомплекс, сопровождающийся ургентностью, ноктурией с сочетанием недержания мочи и учащённым мочеиспусканием или без него при отсутствии доказанной инфекции мочевых путей. Удалось выяснить, что пациенты с данным заболеванием после операции в большей степени страдают недержанием мочи [37]. Следует уделить внимание и возникновению гиперактивности de novo. Данные функциональные изменения возникают из-за денервации и деваскуляризации мочевого пузыря во время выполнения РПЭ [38], хотя в литературе встречаются разные мнения на этот счёт. Так, в исследовании H. Lee et al. не установлено достоверно значимой разницы между инконтинецией после простатэктомии у пациентов с наличием или без гиперактивного мочевого пузыря [39]. В работе S. Song et al. признаки гиперактивности детрузора описаны у 51% прооперированных больных в течение 3 лет. У 27 из 93 пациентов (38%) данные симптомы наблюдались до операции, при этом у 20 из этих 27 (74%) больных типичная симптоматика сохранялась, а иногда и усугублялась в течение 3-летнего наблюдения [38]. Это можно объяснить снижением максимальной ёмкости мочевого пузыря и сфинктерной недостаточностью. В целом, в литературе описывают лишь около 4% случаев НМ после простатэктомии, связанных именно со сфинктерной недостаточностью [40], поэтому не будем выносить этот пункт отдельно.
Перенесенные операции
В некоторых случаях диагноз «Рак предстательной железы» ставится после перенесённого оперативного лечения по поводу гиперплазии простаты, например, после трансуретральной резекции, когда в исследуемом материале морфологи находят злокачественные клетки. В случае, если такому больному в течение 4 месяцев выполняется РПЭ, то риск недержания мочи у такого пациента будет высоким [41]. В других публикациях встречается информация о том, что сам факт перенесённой трансуретральной резекции простаты в анамнезе негативно влияет на удержание мочи после выполнения РПЭ [42]. Впрочем, существует и альтернативное мнение: в исследовании J. R. Palisaar et al. не обнаружено подобной корреляции [43].
Заключение
НМ после перенесённой РПЭ (в т.ч. РАРПЭ) встречается довольно часто, и его негативное влияние на качество жизни пациента очевидно. Несмотря на все плюсы робот-ассистированной РПЭ, нельзя однозначно утверждать, что данная методика позволяет избежать недержания мочи после операции полностью. Возможность на догоспитальном этапе, имея все результаты предоперационных обследований, оценить риски недержания мочи в постоперационном периоде и потенциальный срок восстановления континенции позволяет построить правильную беседу с пациентом. Учитывая то, что в настоящее время больные предъявляют высокие требования не только к онкологическому, но и к функциональному исходу операции, при необходимости можно обсудить менее радикальные варианты лечения, не имеющие таких негативных последствий для больного. Большое количество работ на эту тему, с одной стороны, и взаимоисключающие выводы в исследованиях разных авторов, с другой стороны, лишь подталкивают к дальнейшему изучению этой темы.







